题目内容
在密闭容器中进行如下反应:mA(g)+nB(g)?pC(g),反应经5min达到平衡,测得此时A的浓度减小了a mol?L-1,而C的浓度增加了
a mol?L-1,又知平均反应速率v(C)=2v(B).
(1)写出上述反应的化学方程式______.
(2)压强一定时,C的百分含量(C%)与温度、时间(T表示温度,t表示时间)的关系如图所示.由此可知,该反应为______(填“吸热”或“放热”)反应.
(3)该反应的平衡常数表示式为______,升高温度,K值将______(填“增大”、“减小”或“不变”).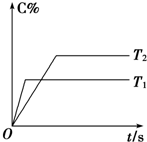
| 2 |
| 3 |
(1)写出上述反应的化学方程式______.
(2)压强一定时,C的百分含量(C%)与温度、时间(T表示温度,t表示时间)的关系如图所示.由此可知,该反应为______(填“吸热”或“放热”)反应.
(3)该反应的平衡常数表示式为______,升高温度,K值将______(填“增大”、“减小”或“不变”).

(1)A的浓度减小了a mol?L-1,C的浓度增加了
a mol?L-1,所以m:p=amol?L-1:
a mol?L-1=3:2,由于v(C)=2v(B),所以p=2n,所以m:n:p=3:1:2,所以方程式为3A(g)+B(g)=2C(g).
故答案为:3A(g)+B(g)=2C(g).
(2)由图可知T1温度先到达平衡,所以温度T1>T2,升高温度,C%减小,平衡向逆反应进行,升高温度平衡吸热反应移动,故正反应为放热反应.
故答案为:放热.
(3)反应3A(g)+B(g)?2C(g)的平衡常数k=
,该反应正反应为放热反应,升高温度平衡向逆反应移动,平衡常数减小.
故答案为:
;减小.
| 2 |
| 3 |
| 2 |
| 3 |
故答案为:3A(g)+B(g)=2C(g).
(2)由图可知T1温度先到达平衡,所以温度T1>T2,升高温度,C%减小,平衡向逆反应进行,升高温度平衡吸热反应移动,故正反应为放热反应.
故答案为:放热.
(3)反应3A(g)+B(g)?2C(g)的平衡常数k=
| c2(C) |
| c3(A)?c(B) |
故答案为:
| c2(C) |
| c3(A)?c(B) |

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
在密闭容器中进行如下反应:X(g)+Y(g)?2Z(g),已知X、Y、Z的起始浓度分别为0.1mol/L、0.2mol/L、0.2mol/L,在一定条件下,达到平衡时,各物质的浓度不可能是( )
| A、Z为0.3 mol/L | B、Y为0.15 mol/L | C、X为0.1 mol/L | D、Z为0.4 mol/L |
在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是( )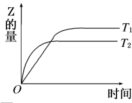

| A、T1<T2,正反应是放热反应 | B、T1<T2,正反应是吸热反应 | C、T1>T2,正反应是放热反应 | D、T1>T2,正反应是吸热反应 |
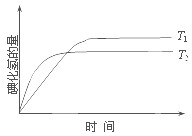 在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g);△H,在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是( )
在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g);△H,在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是( )