题目内容
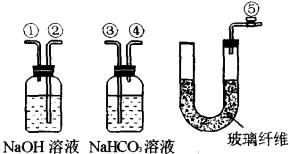
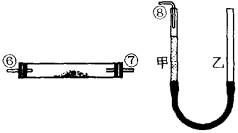
某课外活动小组的学生模拟呼吸面具的原理(过氧化钠与潮湿二氧化碳反应),设计用下列仪器来制取氧气并测量氧气的体积。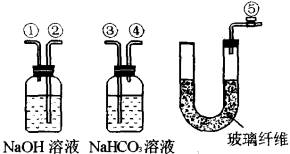
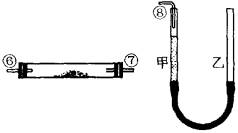
A B C D E
图中量气装置E是由甲、乙两根玻璃管组成,它们用橡胶管连通,并装入适量水。甲管有刻度(0~50mL)供量气用;乙管可上下移动,以调节液面高低。
实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。回答下列问题:
(1)上述装置的连接顺序是(填各接口的编号,其中连接橡胶管及夹持等辅助装置均省略)________。
(2)装置C中放入的反应物是________和________
(3)装置A的作用是________。装置B的作用是________。
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数,求其差值的过程中,应注意________和________(填写字母编号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管波面相平
解析:
| (1)⑤③④⑥⑦②①⑧
(2)大理石、盐酸 (3)吸收O2中的CO2; 吸收CO2中的HCl (4)a c
|
提示:
| 碳酸钠溶于水,反应不易控制;而硫酸可以与大理石反应生成的产物微溶于水,覆盖于大理石的表面,阻止反应继续进行;因此选用大理石和盐酸进行反应制取二氧化碳。
|

实验用品:
仪器:电子天平、砂纸、水槽、100 mL烧杯、铁架台、单孔橡皮塞(玻璃管上带橡胶管和止水夹)、铜丝、30 mL酸式滴定管、100 mL小口径测气管(见下图)。
![]()
药品:镁条、水、15 mol·L-1的浓硫酸。
(1)本实验用0.6 mol·L-1的硫酸进行反应,活动小组共需要480 mL该浓度的硫酸,写出用15 mol·L-1的浓硫酸配制0.6 mol·L-1的硫酸时,还用到的仪器名称和规格____________、____________、____________;需要15 mol·L-1的浓硫酸____________mL。
(2)选用上述仪器的药品进行实验,补写下列实验步骤:
①取一段镁条,擦去氧化膜,称量;
②用细铜丝包裹镁条,铜丝的另一端插在单孔橡皮塞(玻璃管上带橡胶管和止水夹)上;
③_____________________________________________________________;
④_____________________________________________________________;
⑤_____________________________________________________________;
⑥待镁条全部反应后,放置一段时间,调节测气管中水面高度,使管中水面与水槽中水面相平,读出氢气体积。
(3)问题讨论:
①在标准状况下,其他操作都正常,为了保证实验成功,取用的镁条质量应小于_________________g,所用的稀硫酸应大于_________________mL。
②在标准状况下,某学生进行了5次实验,将实验数据通过计算,结果如下:
实验序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
H2的体积(L·mol-1) | 23.45 | 22.41 | 22.38 | 22.39 | 22.42 |
则通过实验验证,标准状况下,1 mol H2的体积为____________L。
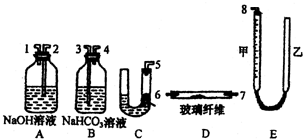 (实验化学)某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积.如图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水.甲管有刻度(0~50mL),供量气用;乙管可上下移动,以调节液面高低.
(实验化学)某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积.如图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水.甲管有刻度(0~50mL),供量气用;乙管可上下移动,以调节液面高低.