题目内容
在室温下,下列叙述正确的是( )
| A.将1 mL 1.0×10-5 mol/L盐酸稀释到1000 mL,得到pH=8 的盐酸 |
| B.将1 mL pH=3的一元酸溶液稀释到10 mL,若溶液的pH<4,则此酸为弱酸 |
| C.用pH=1的盐酸分别中和1 mL pH="13" NaOH溶液和氨水,NaOH消耗盐酸的体积大 |
| D.pH=2的盐酸与pH=1的硫酸比较,2 c(Cl— )=c(SO42— ) |
B
试题分析:盐酸无论怎么稀释,其溶液的pH不可能大于7,A不正确;弱酸存在电离平衡,稀释促进电离,B正确;氨水是弱碱,在pH相等的条件下,氨水的浓度大于氢氧化钠溶液的浓度,C不正确,氨水消耗盐酸的体积大;D不正确,根据电荷守恒可知,c(OH-)+c(Cl—)=c(H+),c(OH-)+2c(SO42—)=c(H+)。所以根据pH=2的盐酸与pH=1的硫酸可,5 c(Cl— )=c(SO42— ),答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的应试能力,提高学生的学习效率。

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
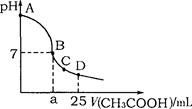
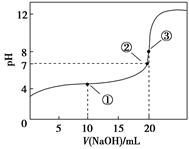
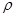 水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。
水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。