题目内容
【题目】25℃,有c(CH3COOH)+c(CH3COO-)=0.1mol/L的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示。下列有关叙述正确的是
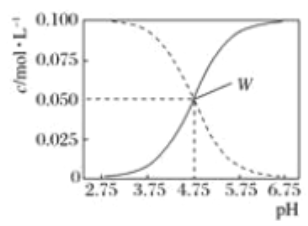
A. pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>>c(H+)>c(OH-)
B. 由图可知该温度下醋酸的电离平衡常数为1×10-5.75
C. pH=3.5溶液中:c(Na+)+ c(H+)-c(OH-)+c(CH3COOH)=0.05mol/L
D. 向1LW点所表示溶液中通入0.05molHCl气体(溶液体积变化可忽略):2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-)+2(Cl-)
【答案】D
【解析】A.根据图象知,pH=5.5溶液中: c(CH3COOH)<c(CH3COO-),A错误;B.W点时c(CH3COOH)=c(CH3COO-),平衡常数![]() ,B错误;C. pH=3.5的溶液中c(Na+)+c(H+)=c(OH-)+c(CH3COO-), 把已知条件c(CH3COOH)+c(CH3COO-)=0.1mol/L代入可得:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol/L,C错误; D.向W点所表示溶液中通入0.05mol HCl气体,原有平衡被打破,建立起了新的平衡,溶液中电荷守恒关系为: c(Na+)+ c(H+)=c(OH-)+c(CH3COO-)+c(Cl-),物料守恒关系为:2c(Na+)= c(CH3COOH)+c(CH3COO-)=0.1mol/L,所以得2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-)+2c(Cl-),D正确;答案选D.
,B错误;C. pH=3.5的溶液中c(Na+)+c(H+)=c(OH-)+c(CH3COO-), 把已知条件c(CH3COOH)+c(CH3COO-)=0.1mol/L代入可得:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol/L,C错误; D.向W点所表示溶液中通入0.05mol HCl气体,原有平衡被打破,建立起了新的平衡,溶液中电荷守恒关系为: c(Na+)+ c(H+)=c(OH-)+c(CH3COO-)+c(Cl-),物料守恒关系为:2c(Na+)= c(CH3COOH)+c(CH3COO-)=0.1mol/L,所以得2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-)+2c(Cl-),D正确;答案选D.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目