题目内容
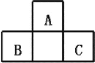
【题目】如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。

已知:铅蓄电池在放电时发生下列电极反应:
负极:Pb+SO42--2e-=PbSO4 正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式__。
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为__极。
(3)用铅蓄电池电解200ml浓度为0.5mol/LCuSO4 溶液一段时间后
①若两极收集到的气体体积相等,则转移电子_____mol。
②阳极收集到的气体体积(标准状况下)为_____L。
【答案】2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑ 正 0.4 2.24
2NaOH+Cl2↑+H2↑ 正 0.4 2.24
【解析】
(1)惰性电极电解饱和食盐水得到氢氧化钠、氢气和氯气;
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明C极为阳极,据此判断铅蓄电池的A极;
(3)用铅蓄电池电解200ml浓度为0.5mol/LCuSO4 溶液一段时间后,阳极只产生氧气,阴极先析出铜、后析出氢气,按电子数守恒及其它已知条件计算即可。
(1)依据电解的原理可得,电解饱和食盐水的化学方程式是:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑;
2NaOH+Cl2↑+H2↑;
(2)惰性电极电解饱和食盐水,阴极水提供的氢离子放电,产生氢气,溶液中氢氧根离子浓度增大,阳极产生氯气,若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明C极为阳极,所以铅蓄电池的A极为正极;
(3)用铅蓄电池电解200ml浓度为0.5mol/LCuSO4 溶液,阳极只产生氧气,阴极先析出铜、后析出氢气;①若两极收集到的气体体积相等,即气体的物质的量相等,则设阳极为: ,阴极析出氢气的物质的量为x,
,阴极析出氢气的物质的量为x, ,则
,则 ,则x=0.1mol,故转移电子的物质的量4x=0.4mol;
,则x=0.1mol,故转移电子的物质的量4x=0.4mol;
②阳极收集到的气体为0.1mol的氧气,标况下的体积为2.24L。

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案