题目内容
10.为探究苯与溴反应的原理,某化学小组设计了如图装置进行实验,实验时,打开分液漏斗活塞,滴加苯和液溴的混合液,反应一段时间后,装置Ⅱ中小试管内有浅红色出现,硝酸银溶液中有淡黄色沉淀生成.根据相关知识回答下列问题:
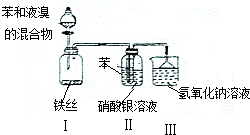
(1)装置Ⅰ中瓶口使用了玻璃塞而不使用橡胶塞,原因是苯与溴的混合物能腐蚀橡胶,装置Ⅰ广口瓶内发生的反应的化学方程式为
 .
.(2)装置Ⅱ内小试管中浅红色的物质是Br2,淡黄色的沉淀是AgBr(填化学式);
(3)装置Ⅲ中倒置漏斗的作用是放倒吸;
(4)若实验时无液溴,但实验室有溴水,获得苯和液溴的混合物的实验方法是萃取.
分析 (1)根据苯与溴的混合物能腐蚀橡胶分析装置Ⅰ中瓶口使用了玻璃塞而不使用橡胶塞原因;苯与溴在三溴化铁作催化剂条件下发生取代反应生成溴苯和溴化氢,据此书写;
(2)根据液溴易挥发,挥发出来的溴易溶于苯,苯与溴在三溴化铁作催化剂条件下发生取代反应生成的溴化氢不溶于苯分析;
(3)根据溴化氢极易溶于水,所以装置Ⅲ中倒置漏斗的作用为放倒吸;
(4)根据溴在苯里溶解性大于在水中的溶解性分析.
解答 解:(1)因为苯与溴的混合物能腐蚀橡胶,所以装置Ⅰ中瓶口使用了玻璃塞而不使用橡胶塞;苯与溴在三溴化铁作催化剂条件下发生取代反应生成溴苯和溴化氢,方程式为 ,故答案为:苯与溴的混合物能腐蚀橡胶;
,故答案为:苯与溴的混合物能腐蚀橡胶; ;
;
(2)因为液溴易挥发,挥发出来的溴易溶于苯,所以装置Ⅱ内小试管内有浅红色出现,则装置Ⅱ内小试管中浅红色的物质是Br2;又苯与溴在三溴化铁作催化剂条件下发生取代反应生成的溴化氢不溶于苯,与硝酸银溶液发生反应生成溴化银的淡黄色的沉淀,所以淡黄色的沉淀是AgBr;
故答案为:Br2;AgBr;
(3)因为溴化氢极易溶于水,所以装置Ⅲ中倒置漏斗的作用为放倒吸;故答案为:放倒吸;
(4)因为溴在苯里溶解性大于在水中的溶解性,所以可以用苯来萃取溴水中的溴,则实验时无液溴,但实验室有溴水,获得苯和液溴的混合物的实验方法是萃取,故答案为:萃取.
点评 本题通过实验主要考查了苯的性质,题目难度中等,注意掌握苯、溴、溴化氢的性质、反应的原理以及熟悉各种仪器的特点和用途是解题的关键,试题充分考查了学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
20. 同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )
同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )
 同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )
同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )| A. | 原子序数:W>Z>X | |
| B. | 气态氢化物的稳定性:N>R | |
| C. | Y和W形成共价化合物 | |
| D. | X和Z两者最高价氧化物对应的水化物能相互反应 |
1.元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分
(1)表中G的元素符号是Al;最易获得电子的元素是氟.(填名称)
(2)下列有关元素性质的递变规律正确的是C
A、氢氧化物的碱性E<F<G
B、获得电子的能力I>J>K
C、气态氢化物的稳定性D>K
D、原子半径H<I<J<K.
| 族 周期 | ⅠA | 0 | ||||||
| ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 2He | ||
| 1 | A | |||||||
| 2 | B | C | D | |||||
| 3 | E | F | G | H | I | J | K | L |
(2)下列有关元素性质的递变规律正确的是C
A、氢氧化物的碱性E<F<G
B、获得电子的能力I>J>K
C、气态氢化物的稳定性D>K
D、原子半径H<I<J<K.
18.下列实验方案能够达到预期目的是( )
| A. | 乙醇的消去反应可用水浴加热 | |
| B. | 检验无水乙醇中是否含有少量水:加硫酸铜晶体观察现象 | |
| C. | 区别苯和乙苯:加酸性高锰酸钾溶液,振荡,观察现象 | |
| D. | 检验氯代烃中的氯元素时,可先加入硝酸溶液,再加入硝酸银溶液来进行检验 |
5.在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)?2C(g),下列说法能证明这一反应已经达到化学平衡状态的是( )
| A. | 单位时间消耗nmol A,同时生成2nmolC | |
| B. | A,B,C的分子数之比为1:2:3 | |
| C. | A,B,C的浓度相等 | |
| D. | 生成C的速率与分解C的速率相等 |
15.与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的化合物是( )
| A. | Na2S | B. | CCl4 | C. | KCl | D. | Na2O |
20.欲制取较纯净的1,2二氯乙烷,可采取的方法是( )
| A. | 乙烯与HCl加成 | |
| B. | 乙烯与Cl2加成 | |
| C. | 乙烷与Cl2按1:2的体积比在光照条件下反应 | |
| D. | 乙烯先与HCl加成,再与等物质的量的Cl2在光照下反应 |
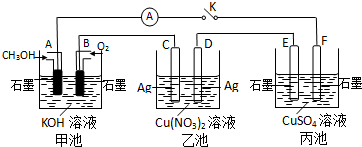
 根据反应:Zn+CuSO4=ZnSO4+Cu,选择适宜的材料和试剂设计一个原电池,完成下列问题:
根据反应:Zn+CuSO4=ZnSO4+Cu,选择适宜的材料和试剂设计一个原电池,完成下列问题: