题目内容
12.高聚酚酯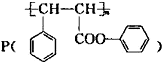 是一种环保型的新涂料,其合成路线如图所示:请回答下列问题:
是一种环保型的新涂料,其合成路线如图所示:请回答下列问题: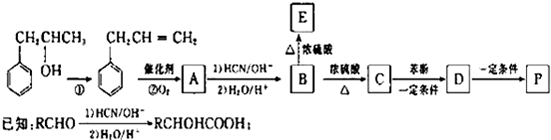
(1)P的分子式为(C15H12O2)n,反应①属于消去反应,反应①还有多种有机副产物,其中能使溴的CCl4溶液褪色的副产物的结构简式为
 .
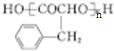
.(2)若反应②中两种反应物物质的量之比为1:1,则除A外另一种产物的名称是甲醛,E是高分子化合物,其结构简式为
 .
.(3)C转化为D的化学方程式是
 .
.(4)B有多种同分异构体,符合下列条件的同分异构体共有23种,其中核磁共振氢谱有6组峰的是
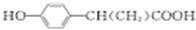 (写出其中一种的结构简式).
(写出其中一种的结构简式).①能与NaHCO3 溶液反应
②遇FeCl3溶液显紫色
③分子中含一个-CH3
(5)由
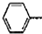 CH2CH=CH2合成B的另一种途径为:
CH2CH=CH2合成B的另一种途径为: CH2CH=CH2$\stackrel{Cl_{2}+CCl_{4}}{→}$F$→_{△}^{NaOH溶液}$H$\stackrel{氧化}{→}$
CH2CH=CH2$\stackrel{Cl_{2}+CCl_{4}}{→}$F$→_{△}^{NaOH溶液}$H$\stackrel{氧化}{→}$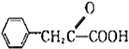 $→_{一定条件}^{G}$
$→_{一定条件}^{G}$则F中官能团名称是氯原子,H的结构简式为
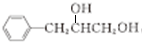 ,试剂G的化学式H2.
,试剂G的化学式H2.
分析 对比结构可知,反应①发生醇的消去反应,由P的结构,逆推可知D为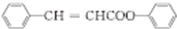 ,进一步反推C为
,进一步反推C为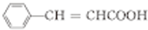 、B为
、B为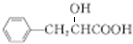 ,A为
,A为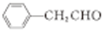 ,由B生成E的反应条件及E是高分子化合物,可知E为
,由B生成E的反应条件及E是高分子化合物,可知E为 .对比结构可知,反应①发生醇的消去反应,还一生成另外一种烯烃:
.对比结构可知,反应①发生醇的消去反应,还一生成另外一种烯烃: .
.
(4)由①能与NaHCO3 溶液反应,可知结构中含有-COOH;②遇 FeCl3溶液显紫色,可知结构中含有苯环且苯环上含有一个-OH,结合③分子中含一个-CH3,可知苯环侧链有以下几种情况:有2个侧链,为-OH、-CH(CH3)COOH,有邻、间、对三种位置;有3个侧链,为-OH、-CH3、-CH2COOH,或者为-OH、-CH2CH3、-COOH,采取定二移一法确定同分异构体数目;
(5)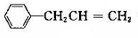 与氯气发生加成反应生成F为
与氯气发生加成反应生成F为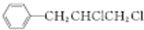 ,F发生水解反应生成H为
,F发生水解反应生成H为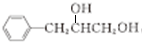 ,H发生氧化反应生成
,H发生氧化反应生成 ,再与氢气发生加成反应生成B.
,再与氢气发生加成反应生成B.
解答 解:由P的结构,逆推可知D为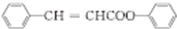 ,进一步反推C为
,进一步反推C为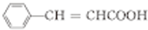 、B为
、B为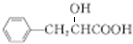 ,A为
,A为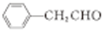 ,由B生成E的反应条件及E是高分子化合物,可知E为
,由B生成E的反应条件及E是高分子化合物,可知E为 .
.
(1)由P的结构简式,可知P的分子式为(C15H12O2)n,对比结构可知,反应①发生醇的消去反应,还一生成另外一种烯烃: ,
,
故答案为:(C15H12O2)n;消去; ;
;
(2)若反应②中两种反应物物质的量之比为1:1,结合A的结构可知为碳碳双键发生断裂生成醛,外另一种产物为HCHO,名称是甲醛,由上述分析剧增,高分子化合物E的结构筒式为 ,
,
故答案为:甲醛; ;
;
(3)C转化为D的化学方程式是: ,
,
故答案为: ;
;
(4)由①能与NaHCO3 溶液反应,可知结构中含有-COOH;②遇 FeCl3溶液显紫色,可知结构中含有苯环且苯环上含有一个-OH,结合③分子中含一个-CH3,可知苯环侧链有以下几种情况:有2个侧链,为-OH、-CH(CH3)COOH,有邻、间、对三种位置;有3个侧链,为-OH、-CH3、-CH2COOH,或者为-OH、-CH2CH3、-COOH,其中2个取代基有邻、间、对3种位置,对应的另外1个取代基分别有4、4、2种位置,每种情况有10种,故共有23种,其中核磁共振氢谱中有6组峰的其中一种的结构简式为: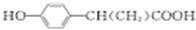 等,
等,
故答案为:23;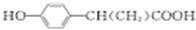 ;
;
(5)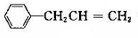 与氯气发生加成反应生成F为
与氯气发生加成反应生成F为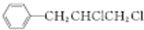 ,含有官能团为氯原子,F发生水解反应生成H为
,含有官能团为氯原子,F发生水解反应生成H为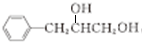 ,H发生氧化反应生成
,H发生氧化反应生成 ,再与氢气发生加成反应生成B,试剂G的化学式H2,
,再与氢气发生加成反应生成B,试剂G的化学式H2,
故答案为:氯原子;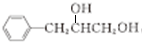 ;H2.
;H2.
点评 本题考查有机物的推断,根据P的结构及反应条件,利用逆推法进行推断,综合考查学生分析推理、知识迁移应用能力,是高考常见题型,难度中等.

| A. | 分子晶体中的每个分子内一定含有共价键 | |
| B. | 原子晶体中的相邻原子间可能存在极性共价键 | |
| C. | 离子晶体中可能含有共价键 | |
| D. | 金属晶体的熔点和沸点都很高 |
| A. | 4 | B. | 4.5 | C. | 5.5 | D. | 6 |
| A. | 44gCO2 的体积为22.4L | |
| B. | 标准状况下,22.4L水中含有NA个水分子 | |
| C. | 常温常压下,28gN2中所含的原子数目为2NA | |
| D. | 如果11.2LN2中含有n个氮气分子,则阿佛加德罗常数一定为2n |
| A. | 在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA | |
| B. | 1 L 1 mol•L-1 NH4NO3溶液中氮原子数小于2NA | |
| C. | 常温常压下,11.2 g乙烯中含有共用电子对数目为2.4NA | |
| D. | 标准状况下,22.4 L CHCl3中所含有的分子数为NA |
| A. | 正极附近的SO42-浓度逐渐增大 | B. | 电子通过导线由铜片流向锌片 | ||
| C. | 正极有O2逸出 | D. | 铜片上有H2逸出 |
| A. | FeSO4 | B. | MgSO4 | C. | AlCl3 | D. | NH4Cl |
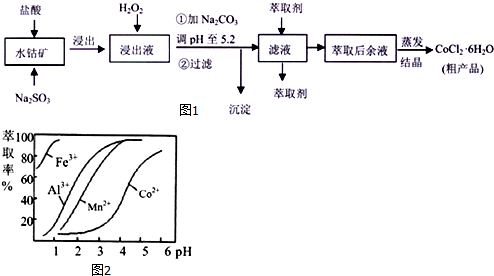
己知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等; ②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)写出浸出液中加氧化剂H202发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)加Na2C03调pH至5.2的目的是完全沉淀Fe3+、Al3+.
(4)萃取剂对金属离子的萃取率与pH的关系如图2.萃取剂的作用是除去溶液中的Mn2+;其使用的较适宜pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
(5)为测定粗产品中CoC12•6H20的含量,称取一定质量的粗产品溶于水,加入足量AgN03溶液,过滤、洗涤,将沉淀烘干后称其质量.若沉淀未烘干就直接称量,则会导致粗产品中CoCl2•6H20的质量分数的计算结果大于实际值(填大于、等于或小于).