题目内容
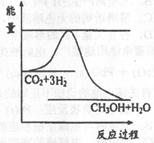
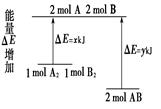
已知反应X+Y= M+N为吸热反应,对这个反应的下列说法中正确的是( )
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.该化学反应进行时,只有能量被吸收,故为吸热反应 |
| D.X和Y的总能量一定低于M和N的总能量 |
D
所谓放热反应即是反应物的总能量高于产物的总能量。

练习册系列答案
相关题目
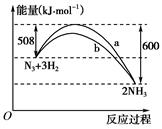
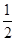 O2(g)=CO2(g) △H= —283kJ/mol
O2(g)=CO2(g) △H= —283kJ/mol H2(g)+CO2(g)△H=
H2(g)+CO2(g)△H= 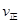 (CO)=
(CO)=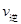 (H2O) d.c(CO)=c(H2)
(H2O) d.c(CO)=c(H2) 
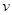 (CO2)表示的反应速率为 。
(CO2)表示的反应速率为 。