题目内容
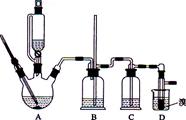
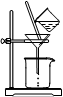
(8分)翰林汇现用MnO2与浓盐酸反应制氯气,再用铜粉和氯气制取少量CuCl2 ,其实验流程示意图如下:

上图中“→”表示气流方向。请完成下列填空。
(1)A 中发生反应的离子方程式为 ;
(2)B中选用的试剂是 ;
(3)D装置中的现象为 ;
(4)若E中的试剂选择KOH溶液,写出相应的吸收反应的化学方程式 。

上图中“→”表示气流方向。请完成下列填空。
(1)A 中发生反应的离子方程式为 ;
(2)B中选用的试剂是 ;
(3)D装置中的现象为 ;
(4)若E中的试剂选择KOH溶液,写出相应的吸收反应的化学方程式 。
(1)MnO2+4H++2Cl- Mn2++Cl2↑+2H2O (2)饱和食盐水
Mn2++Cl2↑+2H2O (2)饱和食盐水
(3)剧烈燃烧,产生棕黄色烟 (4)Cl2+2KOH=KCl+KClO+H2O
 Mn2++Cl2↑+2H2O (2)饱和食盐水
Mn2++Cl2↑+2H2O (2)饱和食盐水(3)剧烈燃烧,产生棕黄色烟 (4)Cl2+2KOH=KCl+KClO+H2O
试题分析:(1)实验室制氯气的离子反应方程式为:MnO2+4H++2Cl-
 Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。(2)B装置是除去Cl2中的HCl,所以用饱和食盐水。
(3)铜与氯气反应的现象是铜丝剧烈燃烧,产生棕黄色烟。
(4)用氢氧化钾吸收氯气的化学方程式为:Cl2+2KOH=KCl+KClO+H2O。
点评:本题主要考查的是实验室制氯气的实验,非常基础简单。

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目