题目内容
下列关于元素周期表、元素周期律的叙述正确的是( )
| A、元素周期表中第一纵行的元素都是碱金属 |
| B、元素的性质随着原子序数的递增而呈周期性变化 |
| C、随着元素原子序数的递增,元素的最高正价从+1到+7,负价从-7到-1重复出现 |
| D、利用周期律,可以在金属与非金属的交界处找到催化剂、耐高温和耐腐蚀的合金材料 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.ⅠA族包含碱金属与氢元素;
B.随原子序数增大,原子核外电子排布呈周期性变化,元素的性质也呈周期性变化;
C.O、F元素没有正化合价;
D.在金属与非金属的交界处寻找半导体材料.
B.随原子序数增大,原子核外电子排布呈周期性变化,元素的性质也呈周期性变化;
C.O、F元素没有正化合价;
D.在金属与非金属的交界处寻找半导体材料.
解答:
解:A.ⅠA族除包含碱金属外,还有氢元素,故A错误;
B.随原子序数增大,原子核外电子排布呈周期性变化,元素的性质也呈周期性变化,故元素的性质随着原子序数的递增而呈周期性变化,故B正确;
C.O、F元素没有正化合价,故C错误;
D.在金属与非金属的交界处元素具有一定的金属性、非金属性,可以在此寻找半导体材料,在过渡元素中寻找催化剂、耐高温和耐腐蚀的合金材料,故D错误,
故选B.
B.随原子序数增大,原子核外电子排布呈周期性变化,元素的性质也呈周期性变化,故元素的性质随着原子序数的递增而呈周期性变化,故B正确;
C.O、F元素没有正化合价,故C错误;
D.在金属与非金属的交界处元素具有一定的金属性、非金属性,可以在此寻找半导体材料,在过渡元素中寻找催化剂、耐高温和耐腐蚀的合金材料,故D错误,
故选B.
点评:本题考查元素周期表与元素周期律,比较基础,注意对基础知识理解掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
铋酸钠(NaBiO3)是一种强氧化剂,可将Mn2+氧化为MnO4-,该反应要在浓HNO3而不是浓盐酸酸化的条件下进行,这是因为( )
| A、HNO3是一种强氧化剂 |
| B、HNO3的酸性比盐酸强 |
| C、Cl-易被强氧化剂氧化 |
| D、NO3-对BiO3-氧化Mn2+有催化作用 |
下列有关化学用语表示正确的是( )
| A、乙酸的结构简式:C2H4O2 |
| B、中子数为20的氯原子:1720Cl |
C、F-的结构示意图: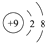 |
D、NH4Br的电子式: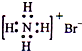 |
鉴别下列各组物质所用方法或试剂不可靠的是( )
| A、用酸性高锰酸钾溶液鉴别乙烷与乙烯 |
| B、用溴水鉴别苯、硝基苯和苯乙烯 |
| C、用燃烧方法鉴别聚乙烯、聚氯乙烯和聚苯乙烯 |
| D、用溴水鉴别苯、甲苯和己烷 |
分子式为C5H8的有机物,其结构不可能的是( )
| A、只含有一个双键的链状有机物 |
| B、含有两个双键的链状有机物 |
| C、含有两个双键的环状有机物 |
| D、含有一个叁键的链状有机物 |
如图是元素周期表前四周期的一部分,关于元素R、W、X、Y、Z的叙述正确的是( )
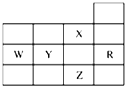

| A、最高价氧化物的水化物的酸性:W>Y |
| B、Z的单质常温下是液体,所在的周期中含有32种元素 |
| C、Z的原子序数比R大17 |
| D、氢化物的沸点:X<Z |
CH4中混有C2H4,欲除去C2H4得到纯净的CH4,最好依次通过盛有下列哪一组试剂的洗气瓶( )
| A、澄清石灰水,浓H2SO4 |
| B、酸性KMnO4溶液,浓H2SO4 |
| C、Br2水,浓H2SO4 |
| D、浓H2SO4,酸性KMnO4溶液 |
下列除杂的方法合理可行的是( )
| A、将混合气体通过灼热的氧化铜除去N2中混有的O2 |
| B、通入足量的CO2可除去NaHCO3溶液中混有的Na2CO3 |
| C、加入浓溴水,再过滤可以除去苯中混有少量的苯酚 |
| D、KNO3溶液中混有少量K2SO4可以通过加入适量BaCl2溶液并过滤来提纯 |