题目内容
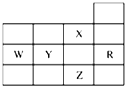
如图是元素周期表前四周期的一部分,关于元素R、W、X、Y、Z的叙述正确的是( )

| A、最高价氧化物的水化物的酸性:W>Y |
| B、Z的单质常温下是液体,所在的周期中含有32种元素 |
| C、Z的原子序数比R大17 |
| D、氢化物的沸点:X<Z |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素在周期表中的位置知,R、W、X、Y、Z分别是Ar、P、F、S、Br元素,
A.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
B.第四周期有18种元素;
C.Z的原子序数比R大17;
D.含有氢键的氢化物沸点较高.
A.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
B.第四周期有18种元素;
C.Z的原子序数比R大17;
D.含有氢键的氢化物沸点较高.
解答:
解:根据元素在周期表中的位置知,R、W、X、Y、Z分别是Ar、P、F、S、Br元素,
A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性Y>W,所以最高价氧化物的水化物的酸性:W<Y,故A错误;
B.Z是溴元素,溴单质常温下呈液态,第四周期有18种元素,故B错误;
C.Z的原子序数是35、R的原子序数是18,所以Z的原子序数比R大17,故C正确;
D.X的氢化物中含有氢键、Z的氢化物中不含氢键,氢键导致氢化物的沸点升高,所以氢化物沸点X>Z,故D错误;
故选C.
A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性Y>W,所以最高价氧化物的水化物的酸性:W<Y,故A错误;
B.Z是溴元素,溴单质常温下呈液态,第四周期有18种元素,故B错误;
C.Z的原子序数是35、R的原子序数是18,所以Z的原子序数比R大17,故C正确;
D.X的氢化物中含有氢键、Z的氢化物中不含氢键,氢键导致氢化物的沸点升高,所以氢化物沸点X>Z,故D错误;
故选C.
点评:本题考查了元素周期表和元素周期律的综合应用,知道元素非金属性与其氢化物的稳定性、其最高价氧化物的水化物酸性关系,注意氢化物沸点高低与氢键、相对分子质量有关,与化学键强弱无关,为易错点.

练习册系列答案
相关题目
在氯化铁和盐酸的混合溶液中,已知c(Cl-)═a mol/L,pH═b<1,则溶液中c(Fe3+)为( )
A、
| ||
| B、(a-1×10-b) mol/L | ||
C、(a-
| ||
| D、上述答案都不正确 |
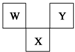 如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )
如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )| A、三种元素的原子半径的大小顺序是W<Y<X |
| B、X元素的氧化物、氢化物的水溶液都呈酸性 |
| C、Y元素的单质是非金属单质中唯一能跟水发生激烈反应的单质 |
| D、W最高价氧化物对应水化物具有强酸性,气态氢化物的水溶液具有弱碱性 |
能正确表示下列反应的离子方程式是( )
| A、硫化氢气体通入硫酸铜溶液中:H2S+Cu2+=CuS↓+2H+ |
| B、铁与足量稀硝酸反应:Fe+4H++NO3-=Fe2++4H2O+NO↑ |
| C、醋酸溶解大理石:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、等物质的量的Ba(OH)2与Al2(SO4)3在溶液中反应:Ba2++3OH-+Al3++SO42-=BaSO4↓+Al(OH)3↓ |
下列关于元素周期表、元素周期律的叙述正确的是( )
| A、元素周期表中第一纵行的元素都是碱金属 |
| B、元素的性质随着原子序数的递增而呈周期性变化 |
| C、随着元素原子序数的递增,元素的最高正价从+1到+7,负价从-7到-1重复出现 |
| D、利用周期律,可以在金属与非金属的交界处找到催化剂、耐高温和耐腐蚀的合金材料 |
下列反应中能用离子方程式:H++OH-═H2O表示的是( )
| A、石灰乳与盐酸溶液反应 |
| B、氢氧化铁与硫酸反应 |
| C、氢氧化钡溶液与硫酸反应 |
| D、氢氧化钠溶液与硫酸反应 |
把物质的量均为0.1mol的CuCl2和H2SO4溶于水制成200mL的混合溶液,用石墨做电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下体积相同(假设溶液体积不变).则下列描述正确的是( )
| A、电路中共转移1.2NA个电子 |
| B、阳极得到的气体中O2的物质量为0.2mol |
| C、阴极质量增加3.2g |
| D、电解后剩余硫酸溶液的浓度为0.5 mol?L-1 |
不能通过一次反应直接实现变化的是( )
①N2→NO2 ②S→SO2 ③NH3→NO ④NO→HNO3 ⑤HNO3→NO.
①N2→NO2 ②S→SO2 ③NH3→NO ④NO→HNO3 ⑤HNO3→NO.
| A、①⑤ | B、②⑤ | C、①④ | D、③④ |