题目内容
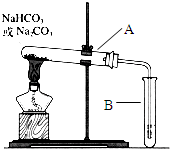 某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案.
某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案.(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成;
(2)设计实验:①利用如图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为
(5)在加热后的A试管中仍留有少量白色固体,冷却后加少量水溶解,再滴加1~2滴酚酞试液,可观察到的现象是
分析:(2)检验二氧化碳的常用试剂为澄清石灰水,二氧化碳与氢氧化钠溶液的反应没有明显现象;
(3)碳酸氢钠分解生成的二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀;
(4)根据反应关系式计算出生成的二氧化碳气体在标况下的体积;
(5)A试管中仍留有少量白色固体为碳酸钠,碳酸钠溶液中碳酸根离子水解,溶液显示碱性.
(3)碳酸氢钠分解生成的二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀;
(4)根据反应关系式计算出生成的二氧化碳气体在标况下的体积;
(5)A试管中仍留有少量白色固体为碳酸钠,碳酸钠溶液中碳酸根离子水解,溶液显示碱性.
解答:解:(2)由于氢氧化钠溶液与二氧化碳的反应没有明显现象,所以无法检验是否有二氧化碳生成,检验二氧化碳气体的常用试剂为澄清石灰水,将二氧化碳气体通入澄清石灰水,澄清石灰水会变浑浊,
故答案为:澄清石灰水;
(3)碳酸钠加热不分解,而碳酸氢钠加热分解生成二氧化碳气体,二氧化碳通入澄清石灰水后,溶液变浑浊,生成了白色沉淀碳酸钙,说明碳酸钠稳定性大于碳酸氢钠,
故答案为:白色;>;
(4)碳酸氢钠分解的关系式为:2NaHCO3~CO2,8.4gNaHCO3的物质的量为0.1mol,完全分解可以生成0.05mol二氧化碳,标况下0.05mol二氧化碳的体积为:22.4L/mol×0.05mol=1.12L,
故答案为:1.12;
(5)反应后A试管中会有少量碳酸钠白色固体,碳酸钠溶液中碳酸根离子部分水解,溶液为碱性,所以滴加1~2滴酚酞试液,溶液显示红色,
故答案为:溶液呈红色.
故答案为:澄清石灰水;
(3)碳酸钠加热不分解,而碳酸氢钠加热分解生成二氧化碳气体,二氧化碳通入澄清石灰水后,溶液变浑浊,生成了白色沉淀碳酸钙,说明碳酸钠稳定性大于碳酸氢钠,
故答案为:白色;>;
(4)碳酸氢钠分解的关系式为:2NaHCO3~CO2,8.4gNaHCO3的物质的量为0.1mol,完全分解可以生成0.05mol二氧化碳,标况下0.05mol二氧化碳的体积为:22.4L/mol×0.05mol=1.12L,
故答案为:1.12;
(5)反应后A试管中会有少量碳酸钠白色固体,碳酸钠溶液中碳酸根离子部分水解,溶液为碱性,所以滴加1~2滴酚酞试液,溶液显示红色,
故答案为:溶液呈红色.
点评:本题考查了碳酸钠、碳酸氢钠的化学性质,题目难度中等,注意掌握碳酸钠、碳酸氢钠的热稳定性大小,能够根据反应方程式进行简单的化学计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
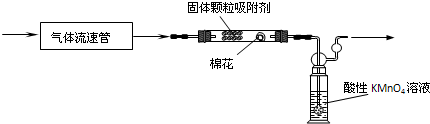
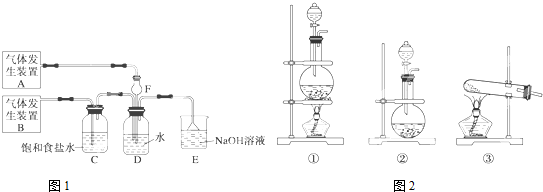
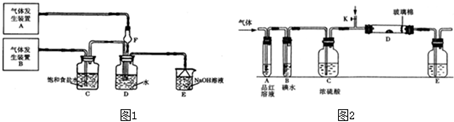
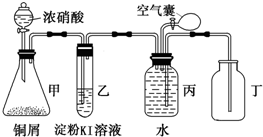 某校化学兴趣小组用所示装置图验证NO2的氧化性和NO的还原性.请回答下列问题:
某校化学兴趣小组用所示装置图验证NO2的氧化性和NO的还原性.请回答下列问题: