题目内容
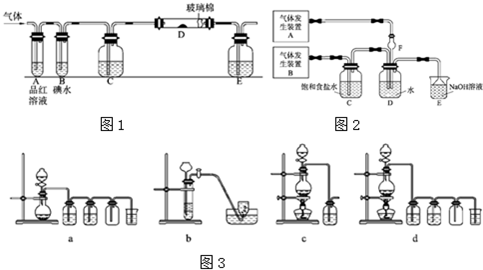
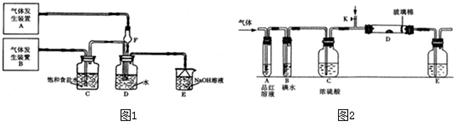
为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图1所示的实验装置.
(1)气体发生装置A产生的气体是 ;
(2)为验证通入D装置中的气体是Cl2过量还是SO2过量,某小组同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液
④苯酚溶液 ⑤品红溶液 ⑥酸性高锰酸钾溶液
I 若Cl2过量:取适量D中溶液滴加至盛有 (选填一个序号)试剂的试管内,再加入 (选填一个序号)试剂,实验现象是: ;
II 若SO2过量:取适量D中溶液滴加至盛有 (选填一个序号)试剂的试管内,实验现象是:
(3)另一小组设计如图所示的装置图2(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);
②若装置B中装有5.0mL 1.0mol/L在碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2mol电子,该反应的化学方程式为 .
(4)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2的与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式 .

(1)气体发生装置A产生的气体是
(2)为验证通入D装置中的气体是Cl2过量还是SO2过量,某小组同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液
④苯酚溶液 ⑤品红溶液 ⑥酸性高锰酸钾溶液
I 若Cl2过量:取适量D中溶液滴加至盛有
II 若SO2过量:取适量D中溶液滴加至盛有
(3)另一小组设计如图所示的装置图2(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?
②若装置B中装有5.0mL 1.0mol/L在碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2mol电子,该反应的化学方程式为
(4)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2的与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式
分析:(1)由装置图可知,A装置产生的气体为二氧化硫;
(2)Ⅰ、氯气过量可以设计实验验证氯气的氧化性,结合亚铁离子被氧化为铁离子后,加入硫氰酸钾溶液会变红色证明;
Ⅱ、二氧化硫过量可以依据二氧化硫具有漂白性或还原性设计实验和选择试剂验证;
(3)①二氧化硫具有漂白性,氯气与水反应生成HClO,HClO具有漂白性;
②通入足量的氯气,碘完全反应,根据转移电子数目计算I元素在氧化产物中的化合价,确定产物,据此书写;
(4)由元素S和O组成-2价酸根离子X,X中S和O的质量比4:3,则N(S):N(O)=
:
=2:3,则X为S2O32-,含S2O32-的溶液与氯气反应,有淡黄色沉淀生成,该淡黄色沉淀为S,上层清液加入氯化钡溶液,有白色沉淀产生,且沉淀加盐酸不溶解,说明生成SO42-,根据氧化还原反应,氯气被还原为氯离子,据此书写.
(2)Ⅰ、氯气过量可以设计实验验证氯气的氧化性,结合亚铁离子被氧化为铁离子后,加入硫氰酸钾溶液会变红色证明;
Ⅱ、二氧化硫过量可以依据二氧化硫具有漂白性或还原性设计实验和选择试剂验证;
(3)①二氧化硫具有漂白性,氯气与水反应生成HClO,HClO具有漂白性;
②通入足量的氯气,碘完全反应,根据转移电子数目计算I元素在氧化产物中的化合价,确定产物,据此书写;
(4)由元素S和O组成-2价酸根离子X,X中S和O的质量比4:3,则N(S):N(O)=
| 4 |
| 32 |
| 3 |
| 16 |
解答:解:(1)由装置图可知,B装置气体生成后通入饱和食盐水中,说明是氯气的发生装置,通过食盐水除去气体中的氯化氢气体,所以A装置产生的气体为二氧化硫,二氧化硫是易溶于水的气体,通过F通入水防止倒吸;
故答案为:SO2;
(2)Ⅰ、为验证通入D装置中的气体是Cl2还是SO2过量,若Cl2过量,取适量D中溶液滴加至盛有氯化亚铁溶液,试剂的试管内,再加入硫氰化钾溶液会变血红色,或加入苯酚溶液变紫色,证明氯气氧化亚铁离子;
故答案为:②;③或④;溶液呈血红色或紫色;
Ⅱ、若SO2过量,取适量D中溶液滴加至盛有品红溶液的试管中或酸性高锰酸钾溶液,试管中现象为红色褪去,加热又恢复红色或溶液变成无色;
故答案为:⑤或⑥;红色褪去为无色,加热后又变为红色或溶液变成无色;
(3)①二氧化硫具有漂白性,氯气与水反应生成HClO,HClO具有漂白性,故通入二氧化硫与通入氯气,装置A中的品红溶液都褪色,故答案为:相同;
②装置B中装有5.0mL 1.0mol?L-1的碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2mol电子,故I元素在氧化产物中的化合价为
=5,故氧化产物为HIO3,氯气被还原为HCl,反应方程式为:5Cl2+I2+6H2O=10HCl+2HIO3;
故答案为:5Cl2+I2+6H2O=10HCl+2HIO3;
(4)由元素S和O组成-2价酸根离子X,X中S和O的质量比4:3,则N(S):N(O)=
:
=2:3,则X为S2O32-,含S2O32-的溶液与氯气反应,有淡黄色沉淀生成,该淡黄色沉淀为S,上层清液加入氯化钡溶液,有白色沉淀产生,且沉淀加盐酸不溶解,说明生成SO42-,根据氧化还原反应,氯气被还原为氯离子,
反应离子方程式为:H2O+S2O32-+Cl2=S↓+SO42-+Cl-+2H+,故答案为:H2O+S2O32-+Cl2=S↓+SO42-+Cl-+2H+.
故答案为:SO2;
(2)Ⅰ、为验证通入D装置中的气体是Cl2还是SO2过量,若Cl2过量,取适量D中溶液滴加至盛有氯化亚铁溶液,试剂的试管内,再加入硫氰化钾溶液会变血红色,或加入苯酚溶液变紫色,证明氯气氧化亚铁离子;
故答案为:②;③或④;溶液呈血红色或紫色;
Ⅱ、若SO2过量,取适量D中溶液滴加至盛有品红溶液的试管中或酸性高锰酸钾溶液,试管中现象为红色褪去,加热又恢复红色或溶液变成无色;
故答案为:⑤或⑥;红色褪去为无色,加热后又变为红色或溶液变成无色;
(3)①二氧化硫具有漂白性,氯气与水反应生成HClO,HClO具有漂白性,故通入二氧化硫与通入氯气,装置A中的品红溶液都褪色,故答案为:相同;
②装置B中装有5.0mL 1.0mol?L-1的碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2mol电子,故I元素在氧化产物中的化合价为
| 5.0×10-2mol |
| 0.005L×1.0mol/L |
故答案为:5Cl2+I2+6H2O=10HCl+2HIO3;
(4)由元素S和O组成-2价酸根离子X,X中S和O的质量比4:3,则N(S):N(O)=
| 4 |
| 32 |
| 3 |
| 16 |
反应离子方程式为:H2O+S2O32-+Cl2=S↓+SO42-+Cl-+2H+,故答案为:H2O+S2O32-+Cl2=S↓+SO42-+Cl-+2H+.
点评:本题考查氯气的制备、对装置的理解与分析、氧化还原反应、氯气与二氧化硫的性质、实验方案设计等,难度中等,(1)中④注意根据电子注意判断I元素在氧化产物中的化合价,是对学生综合能力的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目