题目内容
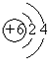
6.(1)某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,其核外电子排布式为[Ar]3d34s2,价电子构型为3d34s2,属d区元素.(2)某元素原子的价电子构型为4s24p1,它属于第四周期ⅢA族,最高正化合价为+3,元素符号是Ga.
(3)原子序数为24的元素原子中有4个能层,7个能级,6个未成对电子.
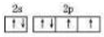
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)
 .
.
分析 (1)最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,应为V,价电子排布式为3d34s2;
(2)元素原子的价电子构型为4s24p1,应为第四周期第ⅢA元素,为Ga元素;
(3)原子序数为24的元素为Cr,原子基态电子排布式为1s22s22p63s23p63d54s1;
(4)2个能层的p轨道中只有一个未成对电子的基态原子为O,外围电子排布为2s22p4.
解答 解:(1)某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,则为第四周期ⅤB的元素V,核外电子排布式为[Ar]3d34s2,价电子排布式为3d34s2,最后填充d电子,为d区元素,
故答案为:[Ar]3d34s2;3d34s2;d;
(2)元素原子的价电子构型为4s24p1,应为第四周期第ⅢA元素,为Ga元素,由最外层电子数可知其最高正化合价为+3价,
故答案为:四;ⅢA;+3;Ga;
(3)原子序数为24的元素为铬,原子基态电子排布式为,1s22s22p63s23p63d54s1,原子核外电子排布分成4层,有4个能层,K能层上有1个能级1s,L能层上有2个能级,分别为2s、2p能级,M能层上有3个能级,分别为3s、3p、3d能级,N能层上有1个能级,为1s,7个能级,3d能级有5个未成对电子,4s1能级,1个未成对电子,共有6个未成对电子,
故答案为:4;7;6;
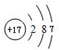
(4)有2个能层且p轨道中只有一对成对电子的基态原子的外围电子排布为2s22p4,外围电子排布图为 ,故答案为:
,故答案为: .
.
点评 本题考查元素的位置、结构,为高频考点,把握原子的结构与元素位置的关系、电子排布等为解答的关键,侧重物质结构与性质的考查,题目难度中等.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
16.下列说法错误的是( )
| A. | 高铁酸钠是一种优良的净水剂 | |
| B. | 锅炉用水的软化可以用阳离子交换法 | |
| C. | 聚氯乙烯塑料薄膜可用于制食品包装袋 | |
| D. | 若镀层被破坏镀锡的铁皮不如镀锌的铁皮耐腐蚀 |
17.下列有关能量变化说法正确的是( )
| A. | 需要加热的化学反应都是吸热反应 | |
| B. | 放热反应都不需要加热就可以发生 | |
| C. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| D. | 化学反应放热还是吸热,取决于反应条件 |
1.下列关于有机化合物性质和结构的叙述中正确的是( )
| A. | 葡萄糖、蔗糖、淀粉都可以食用,都能发生水解 | |
| B. | 苯与液溴在铁作催化剂的条件下的反应为加成反应 | |
| C. | 甲烷、苯、淀粉、蛋白质完全燃烧的产物都只有二氧化碳和水 | |
| D. | 油脂属于酯,在酸性条件下的水解产物都是醇和羧酸 |
11.载人飞船,飞船冲破大气层摆脱地球吸引力,高速运行时会与大气发生摩擦,普通金属材料如钛合金、铝合金摩擦一段时间就会燃烧,因此需要在“神舟七号”的表面涂一层吸热 快、能自动脱落的复合陶瓷,对这种复合陶瓷描述正确的是( )
| A. | 这种复合陶瓷是传统的硅酸盐产品 | |
| B. | 这种复合陶瓷具有耐高温特性、光学特性、生物特性 | |
| C. | 这种陶瓷虽然克服了传统无机非金属材料的缺点,但强度较差 | |
| D. | 这种复合陶瓷具有耐高温、隔热、耐摩擦、硬度大等特点 |
18.下面是某合成高聚物的结构: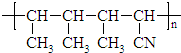 ,该合成高聚物的单体是( )
,该合成高聚物的单体是( )
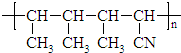 ,该合成高聚物的单体是( )
,该合成高聚物的单体是( )| A. | CH3CH═CHCH3 | B. | CH2═CHCH2CH3 | C. | CH2═CHCH3 | D. | CH3CH═CHCN |
16.下列解释实验现象的反应方程式正确的是( )
| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗 2Na+O2═Na2O2 | |
| B. | 向Na2CO3溶液中滴加稀盐酸起初没看到气体的生成 CO32-+H+═HCO3- | |
| C. | Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物2CO2+2Na2O2═2Na2CO3+O2 | |
| D. | 向NaHCO3溶液中加入过量澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
 、
、