题目内容
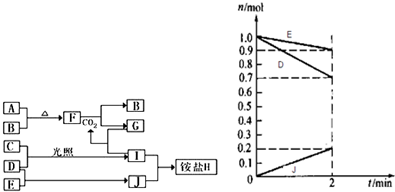
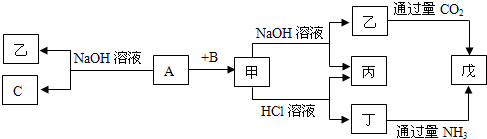
已知化合物A、B、E的焰色反应均为黄色,常温下,A为淡黄色固体,D分子中含有22个电子,由A、B组成的混合物与其他物质间的转化关系如图所示(部分生成物未列出).回答下列问题:
(1)写出A和C的化学式:A______,C______.
(2)混合物中加水后发生反应的化学方程式为:______.
(3)B→D反应的离子方程式为______.

(1)写出A和C的化学式:A______,C______.
(2)混合物中加水后发生反应的化学方程式为:______.
(3)B→D反应的离子方程式为______.
化合物A、B、E的焰色反应均为黄色,都含有Na元素,常温下,A为淡黄色固体,则A为Na2O2,A、B组成的混合物加水生成气体C为O2;含钠化合物B能与硫酸反应生成无色无味气体D,D分子中含有22个电子,D应是CO2,结合由A、B组成的混合物加热可以生成氧气,可推知B为NaHCO3,则E为Na2CO3,
(1)由上述分析可知,A为Na2O2,C为O2,故答案为:Na2O2;O2;
(2)混合物中加水后发生反应的化学方程式为:2Na2O2+4NaHCO3=4Na2CO3+O2↑+2H2O,故答案为:2Na2O2+4NaHCO3=4Na2CO3+O2↑+2H2O;
(3)B→D反应的离子方程式为:CO32-+2H+=CO2↑+H2O,故答案为:CO32-+2H+=CO2↑+H2O.
(1)由上述分析可知,A为Na2O2,C为O2,故答案为:Na2O2;O2;
(2)混合物中加水后发生反应的化学方程式为:2Na2O2+4NaHCO3=4Na2CO3+O2↑+2H2O,故答案为:2Na2O2+4NaHCO3=4Na2CO3+O2↑+2H2O;
(3)B→D反应的离子方程式为:CO32-+2H+=CO2↑+H2O,故答案为:CO32-+2H+=CO2↑+H2O.

练习册系列答案
相关题目