题目内容
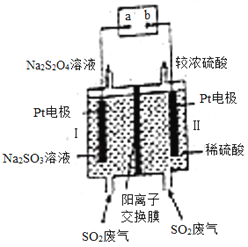
【题目】某学习小组设计实验探究H2S的性质。实验室用硫化亚铁(难溶,块状)与盐酸反应制备硫化氢。他们设计装置如图所示。

回答下列问题:
(1)停止A中反应的操作是________________。
(2)试制X可能是______(填代号)。
(a)氢氧化钠溶液 (b)硝酸 (c)饱和NaHS溶液 (d)氯化铁溶液
(3)写出A中发生反应的离子方程式:_________________。
(4)若E中产生浅黄色沉淀,则氧化性:Cl2____ S(填“>”“<”或“==”)。
(5)若观察到D中紫红色溶液变为无色溶液,则表明H2S具有的性质有_____(填代号)。
(a)酸性 (b)氧化性 (c)不稳定性 (d)还原性
(6)为了证明F中有Fe2+生成,取少量F中溶液于试管,微热溶液,冷却,向试管中滴加下列试剂中的____。(填代号)
①KSCN 溶液 ②酸化的双氧水 ③酸性高锰酸钾溶液 ④氢氧化钠溶液
【答案】关闭K活塞 c FeS+2H+=Fe2++H2S↑ > d ③
【解析】
(1)要停止A中反应的操作是关闭K活塞;(2)试制X是为了除去挥发出来的HCl,又要不与H2S反应,(a)氢氧化钠溶液能吸收H2S,故错误;(b)硝酸能将H2S氧化,故错误; (c)饱和NaHS溶液能吸收HCl,又不与H2S反应,故正确;(d)氯化铁溶液能将H2S氧化,故错误;故选C。(3)A中制取H2S的离子方程式:FeS+2H+=Fe2++H2S↑;(4)若E中产生浅黄色沉淀,发生H2S+Cl2=2HCl+S↓,反应中氧化剂的氧化性大于氧化产物:Cl2> S;(5)若观察到D中紫红色溶液变为无色溶液,则表明H2S具有的性质有还原性,5H2S+8MnO4-+16H+=8Mn2++5SO42-+13H2O故选d;(6)2Fe3++H2S=2Fe2++S↓+2H+,溶液中存在Fe2+,取少量F中溶液于试管,微热溶液,冷却,向试管中滴加下列试剂中的酸性高锰酸钾溶液,紫红色褪去,故选③。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案