��Ŀ����
����Ŀ���˿���Դ����ίԱ�ḱ���Ρ��й���ѧԺԺʿ�ش�ӱ�ʾ����ǰ�����ɢ��ú��û������ú������й������������߶�����������Ҫԭ��ú�������ǽ����������������ú̿����Ҫ;��֮һ��
����֪:H2O(g)=H2O(I) ��H=-44kJ/mol
���� | H2(g) | C(s) | CO(g) |
ȼ����kJ/mol | -285.8 | -393.5 | -283.0 |
����д��ú��������Ӧ���ɺϳ���(CO��H2)���Ȼ�ѧ����ʽ___________��
���ں��¡����ݵķ�Ӧ���У��ܱ���������Ӧ�ﵽƽ��״̬����_______��
a.�������ƽ����Է����������ٸı�
b.����ѹǿ���ٸı�
c.������Ũ�����
d.��Ӧ��ϵ���¶ȱ��ֲ���
e.���������������Ƕ�����������ʵ�2��
f.��������ܶȲ���
g.��λʱ���ڣ�����ˮ������������������������Ϊ9��1
���ڴ��������ºϳ����ϳɼ�������лᷢ�����·�Ӧ��
I CO(g)+3H2(g) = CH4(g)+H2O(g) ��H1= -206 kJ/mol
II CO(g)+H2O(g) = CO2(g)+H2(g) ��H2= -41 kJ/mol
�� 2CO(g)+2H2(g)= CH4(g)+CO2(g) ��H 3= -247.4 kJ/mol
��ͼ1��̫ԭ������ѧú�����о�����������ѧ���ݷ����õ��¶ȶԷ�Ӧ��InK(��ѧƽ�ⳣ��K����Ȼ����)������ͼ,����������������Ƶ�ԭ����____________��

������鷴Ӧѡ���ԵĹؼ�������_______���������֪ʶ��ͼ2�����ϳɼ������˵ķ�Ӧ������
��550��630K��1MPa��ԭ����__________________��
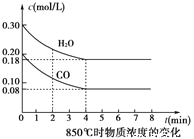
��850��ʱ�����Ϊ5L��Ӧ���з�����Ӧ��CO��H2O(g)Ũ�ȱ仯��ͼ��ʾ������ʽ����������µ�ƽ�ⳣ��_____________ ��
(3)CH4ȼ�ϵ�������ʺܸߣ�װ��������1L2mol/L��KOH��ҺΪ����ʣ���������ͨ���״���¼���22.4L��33.6 Lʱ�����缫��ӦΪ___________��
���𰸡� C(s)+H2O(g)=CO(g)+H2(g) ��H=+131.31kJ/mol abef ��������������ʱ,�¶����߷�ӦI�����ȵ��淴Ӧ�����ƶ�ʹInK��С ���� �������·�Ӧ���ʽϿ���Ҽ�����ʽϸ� K= ![]() =
=![]() =1 CH4-8e-+9CO32-+3H2O=10HCO3-
=1 CH4-8e-+9CO32-+3H2O=10HCO3-
���������Ţ���֪����H2O(g)=H2O(I) ��H1= -44kJ/mol ��H2(g)+![]() O2(g)=H2O(l) ��H2= -285.8kJ/mol ��C(s)+O2(g)=CO2 ��H3= -393.5 kJ/mol ��CO(g)
O2(g)=H2O(l) ��H2= -285.8kJ/mol ��C(s)+O2(g)=CO2 ��H3= -393.5 kJ/mol ��CO(g)![]() O2(g)=CO2 ��H4= -283.0 kJ/mol�����ݸ�˹������+��-��-���ɵ�C(s)+H2O(g)=CO(g)+H2(g) ����H=��+��-��-��=( -393.5 kJ/mol)+(-44kJ/mol)-(-285.8kJ/mol)-(-283.0 kJ/mol)=+131.31kJ/mol����ú��������Ӧ���ɺϳ���(CO��H2)���Ȼ�ѧ����ʽΪC(s)+H2O(g)
O2(g)=CO2 ��H4= -283.0 kJ/mol�����ݸ�˹������+��-��-���ɵ�C(s)+H2O(g)=CO(g)+H2(g) ����H=��+��-��-��=( -393.5 kJ/mol)+(-44kJ/mol)-(-285.8kJ/mol)-(-283.0 kJ/mol)=+131.31kJ/mol����ú��������Ӧ���ɺϳ���(CO��H2)���Ȼ�ѧ����ʽΪC(s)+H2O(g)![]() CO(g)+H2(g) ��H=+131.31kJ/mol��
CO(g)+H2(g) ��H=+131.31kJ/mol��
����֪C(s)+H2O(g)![]() CO(g)+H2(g) ��Ӧ������һ���ǹ��壬�����﷽�����������ķ���a.����������������������ʵ����Dz�ȷ��ֵ�����������ƽ����Է����������ٸı�ʱ��ƽ��״̬����a��ȷ��b.��Ӧ�������������ʵ����Dz�ȷ����ֵ��������ѹǿ���ٸı�ʱ��˵�����������ʵ������ٸı䣬��ƽ��״̬����b��ȷ��c.������Ũ�����ʱ��һ����ƽ��״̬����c����d.�����������¶ȱ��ֲ��䣬��ϵ��һ���ﵽƽ�⣬��d����e.���������������Ƕ�����������ʵ�2����˵���ﵽƽ��״̬����e��ȷ��f.��������ܶȲ��䣬˵�������������������ʱ��ı仯���仯����ƽ��״̬����f��ȷ��g.��λʱ���ڣ�����ˮ������������������������Ϊ9��1����Ϊ����Ӧ���ʣ����ж���ƽ��״̬����g����Ϊabef��
CO(g)+H2(g) ��Ӧ������һ���ǹ��壬�����﷽�����������ķ���a.����������������������ʵ����Dz�ȷ��ֵ�����������ƽ����Է����������ٸı�ʱ��ƽ��״̬����a��ȷ��b.��Ӧ�������������ʵ����Dz�ȷ����ֵ��������ѹǿ���ٸı�ʱ��˵�����������ʵ������ٸı䣬��ƽ��״̬����b��ȷ��c.������Ũ�����ʱ��һ����ƽ��״̬����c����d.�����������¶ȱ��ֲ��䣬��ϵ��һ���ﵽƽ�⣬��d����e.���������������Ƕ�����������ʵ�2����˵���ﵽƽ��״̬����e��ȷ��f.��������ܶȲ��䣬˵�������������������ʱ��ı仯���仯����ƽ��״̬����f��ȷ��g.��λʱ���ڣ�����ˮ������������������������Ϊ9��1����Ϊ����Ӧ���ʣ����ж���ƽ��״̬����g����Ϊabef��
�Ƣ�CO(g)+3H2(g) = CH4(g)+H2O(g) ��H1= -206 kJ/mol�˷�Ӧ�������Ƿ��ȷ�Ӧ���������������������£������¶�ƽ�������ƶ���ƽ�ⳣ�����٣�InKҲ��С��
������ֻ�ı䷴Ӧ���ʣ���Ӱ��ƽ����ƶ���������鷴Ӧѡ���ԵĹؼ����أ��������֪ʶ��ͼ2��������550��630K��1MPa�������·�Ӧ���ʽϿ���Ҽ�����ʽϸ��Ǻϳɼ������˵ķ�Ӧ������
�� CO(g)+H2O(g) ![]() CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼŨ�ȣ�mol/L�� 0.20 0.30 0 0
�仯Ũ�ȣ�mol/L�� 0.12 0.12 0.12 0.12
ƽ��Ũ�ȣ�mol/L�� 0.08 0.18 0.12 0.12
50��ʱ�����µ�ƽ�ⳣ��K= ![]() =
=![]() =1��
=1��
(3)n��KOH��=2mol/L��1L=2mol����װ����ȼ�ϵ�أ������ϼ���ʧ���ӷ���������Ӧ�������������õ��ӷ�����ԭ��Ӧ��22.4L��V��33.6Lʱ������ԭ���غ��1mol��n��CO2����1.5mol����Ӧ����̼����أ�������ӦʽΪCH4-8e-+9CO32-+3H2O=10HCO3-��

����Ŀ����50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺

��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ��������� ��
��2�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ (�ƫ��ƫС����Ӱ�족)
��3�������60mL0.50mol/L������50mL0.55mol/LNaOH��Һ���з�Ӧ��������ʵ����ȣ����ų������� (���ȡ�����ȡ�)�������к��ȡ�H_____ (���ȡ�����ȡ�)
��4���������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬������к��ȡ�H�� (�ƫ����ƫС��������Ӱ�족) ����KOH����NaOH��ʵ�������������_________________(�ƫ����ƫС��������Ӱ�족)��
��5�����Ǽ�¼��ʵ���������£�
ʵ����Ʒ[ | ��Һ�¶� | �к��� ��H | |||
��ʼƽ ���¶� | ��Ӧ����¶� | ||||
�� | 50mL��0.55mol.L-1NaOH | 50mL��0.5mol.L-1HCl | 20�� | 23.3�� | |
�� | 50mL��0.55mol.L-1NaOH | 50mL��0.5mol.L-1HCl | 20�� | 23.5�� | |
��֪��Ӧ����Һ�ı�����CΪ4.18KJ����-1�� Kg-1�������ʵ��ܶȾ���Ϊ1g��cm-3��
�ٸ����ϱ����ݼ����к��ȡ�H=__________(������С�����һλ)
�ڸ���ʵ����д��NaOH��Һ��HCl��Һ��Ӧ���Ȼ�ѧ����ʽ�� ��
��6������ʵ����ֵ�����57.3 kJ/mol��ƫ�����ƫ���ԭ�������(����ĸ)_______________��
A��ʵ��װ�ñ��¡�����Ч����
B����ȡϡ������Һ�����ʱ���Ӷ���
C��һ����NaOH��Һ����ʢ�������С�ձ���
D�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨHCl��Һ���¶�