题目内容
【题目】(1)现有氧化还原反应:3H2O2 + 2H2CrO4 =2Cr(OH)3 + 3O2 ↑+ 2H2O
①用单线桥标出反应中的电子转移数目和方向_____________;
②其中Cr被___________,H2O2作___________剂;
③反应转移了0.3mol电子,则产生的气体在标准状态下体积约为__________。
(2)①将用砂纸打磨过的铝片用坩埚钳夹住在酒精灯上点燃,现象是:________;
②在试管中加入少量Na2O2再加入少量水,用带火星的木条伸入试管,再滴入几滴酚酞,可观察到的现象是_________。
【答案】![]() 还原 还原 3.36L 铝熔化但是不滴落 有大量气泡产生,带火星的木条复燃,滴入酚酞后溶液先变红后褪色
还原 还原 3.36L 铝熔化但是不滴落 有大量气泡产生,带火星的木条复燃,滴入酚酞后溶液先变红后褪色
【解析】
(1)①用单线桥标出反应中的电子转移数目和方向,单箭头从双氧水中-1价的氧出发,到H2CrO4中+6价的铬结束,共转移6个电子,![]() ;故答案为:
;故答案为:![]() ;
;
②其中Cr从+6价降为+3价,被还原,H2O2中-1价的氧化合价升高,失电子,作还原剂;故答案为:还原;还原;
③从3H2O2+ 2H2CrO4=2Cr(OH)3+ 3O2 ↑+ 2H2O得:每转移6mol电子生成3molO2,反应转移了0.3mol电子,生成的氧气的物质的量为:![]() ×3mol=0.15mol,则产生的气体在标准状态下体积约为0.15mol×22.4L·mol-1=3.36L。故答案为:3.36L;
×3mol=0.15mol,则产生的气体在标准状态下体积约为0.15mol×22.4L·mol-1=3.36L。故答案为:3.36L;
(2)①将用砂纸打磨过的铝片用坩埚钳夹住在酒精灯上点燃,铝箔表面在加热时与O2发生反应生成熔点很高的Al2O3薄膜,使内部的铝被Al2O3包裹着,所以熔化的铝不易滴下,现象是:铝熔化但是不滴落;故答案为:铝熔化但是不滴落;
②在试管中加入少量Na2O2再加入少量水生成氢氧化钠和双氧水,氢氧化钠是强碱,双氧水部分分解生成氧气,双氧水有强氧化性和漂白性。因此,用带火星的木条伸入试管,再滴入几滴酚酞,可观察到的现象是:有大量气泡产生,带火星的木条复燃,滴入酚酞后溶液先变红后褪色。故答案为:有大量气泡产生,带火星的木条复燃,滴入酚酞后溶液先变红后褪色。

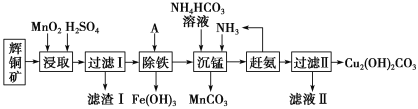
【题目】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为 Cu2S,含少量 Fe2O3、SiO2 等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
已知:
①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
②Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有____(任写一种)。
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的化学方程式:____。
(3)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为____,若加 A 后溶液的 pH调为5,则溶液中 Fe3+的浓度为____mol/L。
(4)写出“沉锰”(除 Mn2+)过程中反应的离子方程式:____。
(5)“赶氨”时,最适宜的操作方法是____。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是____(写化学式)。
(7)过滤Ⅱ得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是____。
【题目】氟化铬可用作毛织品防蛀剂、卤化催化剂、大理石硬化及着色剂。以铬云母矿石(含4.5%Cr2O3,还含Fe2O3、FeO、MgO、SiO2)为原料制备氟化铬的工艺流程如图。
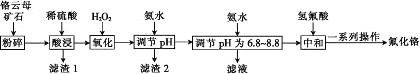
表中列出了相关金属离子生成氢氧化物沉淀的pH:
氢氧化物 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 | Fe(OH)2 |
开始沉淀的pH | 2.3 | 8.8 | 4.9 | 7.5 |
沉淀完全的pH | 4.1 | 10.4 | 6.8 | 9.7 |
请回答下列问题:
(1)Fe2O3、MgO、FeO、SiO2中属于碱性氧化物的有________种。
(2)将铬云母矿石粉碎的目的是________。
(3)滤渣1主要成分的用途是________。(写一种)
(4)Cr2O3与稀硫酸反应的化学方程式为___________。
(5)第一次滴加氨水调节pH范围为________。
(6)第二次滴加氨水调节pH为6.8~8.8的目的是_______,Cr(OH)3与 Al(OH)3一样具有两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH)3会部分溶解,写出Cr(OH)3溶解的离子方程式:________。