题目内容
【题目】离子反应是中学化学中重要的反应类型.回答下列问题:
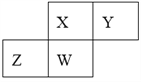
(1)人们常用图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为下左图,下右图为离子反应、氧化还原反应和置换反应三者之间的关系,则表示离子反应、氧化还原反应、置换反应的字母分别是________。
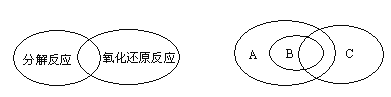
(2)将NaBr溶液加入AgCl沉淀中,产生AgBr黄色沉淀.从离子反应发生的条件分析,AgCl与AgBr相比较,溶解度较大的是________。
(3)离子方程式是重要的化学用语,下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。反应物从下列物质中选取:Na、Fe、H2O、H2SO4、HCl、NaOH、Ba(OH)2、CuCl2(已知2Na+2H2O=2NaOH+H2↑)。
错误观点 | 离子方程式 | |
① | 所有的离子方程式均可以表示一类反应 | _____ |
② | 所有酸碱中和反应均可表示为:H++OH-=H2O | _____ |
【答案】C、A、B AgCl 2Na+2H2O=2Na++2OH-+H2↑ 2H++SO42—+Ba2++2OH-=BaSO4↓+2H2O
【解析】
(1)所有的置换反应全是氧化还原反应,置换反应中有部分是离子反应,部分是非离子反应,氧化还原反应中,有部分是离子反应,部分是非离子反应;
(2)根据离子反应的发生条件可知,离子反应向更难溶的方向移动;
(3)①离子反应可以表示一类反应,但是有的离子反应只表示一个化学反应;
②离子方程式H++OH-=H2O表示强酸和强碱反应生成可溶性的盐和水的中和反应,不能表示强酸和强碱反应生成难溶性的盐和水的中和反应。
(1)所有的置换反应全是氧化还原反应,置换反应中有部分是离子反应,部分是非离子反应,氧化还原反应中,有部分是离子反应,部分是非离子反应,所有的置换反应全是氧化还原反应,是被包含和包含的关系,则A是氧化还原反应,B是置换反应,C是离子反应,故答案为:C、A、B;
(2)根据离子反应的发生条件可知,离子反应向更难溶的方向移动,则将NaBr溶液加入AgCl沉淀中,AgCl白色沉淀转化为AgBr浅黄色沉淀,说明AgCl的溶解度大于AgBr的溶解度,故答案为:,AgCl;
(3)①离子反应可以表示一类反应,但是有的离子反应只表示一个化学反应,比如2Na+2H2O=2Na++2OH-+H2↑只能表示钠和水的反应,故答案为:2Na+2H2O=2Na++2OH-+H2↑;
②离子方程式H++OH-=H2O表示强酸和强碱反应生成可溶性的盐和水的中和反应,不能表示强酸和强碱反应生成难溶性的盐和水的中和反应,比如硫酸和氢氧化钡之间的反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O。