题目内容
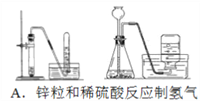
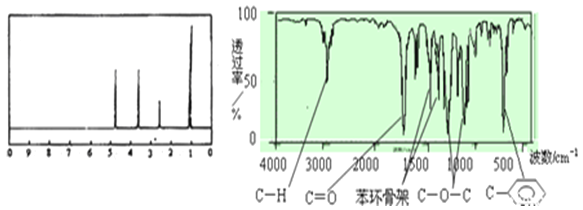
【题目】如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),向20mL0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液 , 根据图示判断,下列说法正确的是( )

A. H2A在水中的电离方程式是:H2A===H++HA-;HA-![]() H++A2-
H++A2-
B. 当V(NaOH)=20 mL时,溶液中各离子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C. 当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2c(OH-)
D. 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
【答案】B
【解析】A. 据图可知,当V(NaOH)=20mL时,发生的反应为:NaOH+H2A=NaHA+H2O,溶质主要为NaHA,此时溶液中同时存在HA、A2和H2A,说明H2A是一种二元弱酸,则H2A在水中的电离方程式为:H2A![]() H++HA、HA
H++HA、HA![]() H++A2,故A错误;B. 当V(NaOH)=20mL时,发生的反应为:NaOH+H2A=NaHA+H2O,溶质主要为NaHA,据图可知,此时溶液中c(A2)>c(H2A),说明HA的电离程度大于水解程度,溶液显酸性,则c(Na+)>c(HA)>c(H+)>c(A2)>c(OH),故B正确;C. 当V(NaOH)=30mL时,发生的反应为:NaOH+H2A=NaHA+H2O、NaHA+NaOH=Na2A+H2O,溶液为等物质的量浓度的NaHA和Na2A的混合溶液,根据电荷守恒得:c(Na+)+c(H+)=c(HA)+2c(A2)+c(OH),根据物料守恒得:3c(HA)+3c(A2)+3c(H2A)=2c(Na+),联立两式得:2c(H+)+c(HA)+3c(H2A)=c(A2)+2c(OH),故C错误;D. 由图示关系可知,等体积等浓度的NaOH溶液与H2A溶液混合后得到NaHA溶液,此时溶液中的c(A2)>c(H2A),说明HA的电离程度大于水解程度,溶液显酸性,水的电离受到抑制,所以等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水小,故D错误;答案选B。
H++A2,故A错误;B. 当V(NaOH)=20mL时,发生的反应为:NaOH+H2A=NaHA+H2O,溶质主要为NaHA,据图可知,此时溶液中c(A2)>c(H2A),说明HA的电离程度大于水解程度,溶液显酸性,则c(Na+)>c(HA)>c(H+)>c(A2)>c(OH),故B正确;C. 当V(NaOH)=30mL时,发生的反应为:NaOH+H2A=NaHA+H2O、NaHA+NaOH=Na2A+H2O,溶液为等物质的量浓度的NaHA和Na2A的混合溶液,根据电荷守恒得:c(Na+)+c(H+)=c(HA)+2c(A2)+c(OH),根据物料守恒得:3c(HA)+3c(A2)+3c(H2A)=2c(Na+),联立两式得:2c(H+)+c(HA)+3c(H2A)=c(A2)+2c(OH),故C错误;D. 由图示关系可知,等体积等浓度的NaOH溶液与H2A溶液混合后得到NaHA溶液,此时溶液中的c(A2)>c(H2A),说明HA的电离程度大于水解程度,溶液显酸性,水的电离受到抑制,所以等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水小,故D错误;答案选B。

 名校课堂系列答案
名校课堂系列答案【题目】Na2O2可用作制氧剂、漂白剂。
(1)已知:2CrO42ˉ+2H+![]() Cr2O72ˉ+H2O。在碱性溶液中,Na2O2可以把Cr2(SO4)3中的Cr元素氧化成+6价,该反应的离子方程式为___________________________________。
Cr2O72ˉ+H2O。在碱性溶液中,Na2O2可以把Cr2(SO4)3中的Cr元素氧化成+6价,该反应的离子方程式为___________________________________。
(2)某化学兴趣小组同学欲在实验室中制备少量Na2O2。
查阅资料得知,将钠加热至熔化,通入一定量的除去CO2的空气,维持温度在453—473K之间,钠即被氧化为Na2O;进而增加空气流量并迅速提高温度至573—673K,即可制得Na2O2。
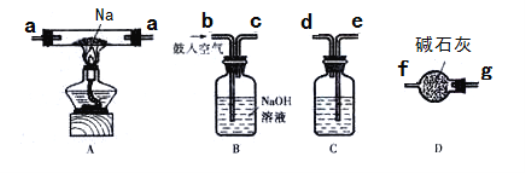
①若采用上述仪器装置制备Na2O2,从左到右仪器的连接顺序为(填接口字母,各装置只能用一次)________;装置D的作用为________。
②装置A中生成Na2O2的化学反应方程式为_______________________。
③若实验时准确称取2.3 gNa进行反应,将反应后的固体溶于1L水中,向所得溶液中加入50 mL 0.5 mol/L NH4Al(SO4)2溶液充分反应,请写出加入NH4A1(SO4)2溶液后发生反应的离子方程式________。
(3)小组同学继续对反应后固体的组成进行探究。
a.取一定量反应后固体,加入足量水充分反应,有气体生成;
b.将生成的气体全部转入真空密闭容器中,放电后充分反应,气体体积减少了3 / 5(不考虑O3的生成)。
①反应后固体中一定有的物质为________(填化学式)。
②为进一步确定反应后固体的组成,需对b中剩余气体继续进行猜想与设计,请完成下表。
猜想 | 实验设计 | 现象与结论 |
剩余气体为___________。 | _______________________________。 | 若看到____________ 证明此猜想正确,反之则不正确 |