题目内容
5.下列有关叙述正确的是( )| A. | Na2O•SiO2是一种简单的硅酸盐,可溶于水 | |
| B. | 严重影响我国北方的霾尘,其颗粒物是种胶体 | |
| C. | 盐酸、NaCl溶液是实验室常见的电解质 | |
| D. | 酸性氧化物均能与水反应生成对应的酸,如CO2、SO3等 |
分析 A、钠盐都是易溶于水的化合物;
B、霾尘直径小于或等于2.5微米即2500nm的细颗粒物(即PM2.5),胶体的分散质粒子直径大小:1nm~100nm;
C、电解质属于化合物,不属于其他范畴;
D、酸性氧化物是指能和碱反应生成盐和水的氧化物.
解答 解:A、Na2O•SiO2是硅酸钠的氧化物表现形式,硅酸钠是一种简单的硅酸盐,可溶于水,故A正确;
B、霾尘直径小于或等于2.5微米即2500nm的细颗粒物(即PM2.5),而胶体的分散质粒子直径大小:1nm~100nm,所以霾尘不一定是胶体,故B错误;
C、氯化钠溶液属于混合物,不属于电解质,故C错误;
D、酸性氧化物是指能和碱反应生成盐和水的氧化物,不一定都能和水反应得到相应的酸,如二氧化硅,故D错误.
故选A.
点评 本题考查学生电解质、酸性氧化物的概念以及钠盐的溶解性、胶体的特点等知识,属于综合知识的考查,难度中等.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
15.下列有机化合物的性质能体现是羟基对苯环产生影响的是( )
| A. | 苯酚溶液显弱酸性 | |
| B. | 苯酚比苯容易发生溴代反应 | |
| C. | 苯酚能与氢氧化钠溶液反应,而苯甲醇不能 | |
| D. | 苯酚和乙醇在60℃的水浴中,分别加入金属钠,苯酚中明显反应剧烈 |
16.下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是( )
| A. | 半导体材料碳化硅 | B. | 超导材料铜锌合金 | ||
| C. | 透明陶瓷材料硒化锌 | D. | 超导材料Cs3C60 |
13.已知室温时,0.1mo1/L某一元酸HX有0.1%发生电离,下列叙述错误的是( )
| A. | 该溶液的pH=4 | |
| B. | 适当升高温度,溶液的pH不变 | |
| C. | 此酸的电离平衡常数约为1×10-7 | |
| D. | 由HX电离出的c(H+)约为水电离出的c(OH-)的106倍 |
20.已知1molR2-中含质子16mol,一定质量的R2-中共含质子8mol,则其中所含的电子的物质的量为( )
| A. | 10 mol | B. | 9 mol | C. | 8 mol | D. | 7 mol |
17.下列说法正确的是( )
| A. | 同温同压下,物质的物质的量越大,体积也越大 | |
| B. | 同温同压下,气体的物质的量越大,体积也越大 | |
| C. | 同温同压下,同体积的气体具有相同的原子数 | |
| D. | 体积相同的气体,所含分子数也相同 |
2.某小组利用如图1装置,用苯与溴在FeBr3催化作用下制备溴苯:
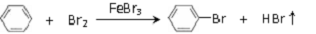
反应剧烈进行,烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现,蒸馏水逐渐变成黄色.反应停止后按
如图2流程分离产品:
已知:溴苯难溶于水,与有机溶剂互溶;溴、苯、溴苯的沸点依次为59℃、80℃、156℃.
(1)操作Ⅰ为过滤,操作Ⅱ为蒸馏.
(2)“水洗”、“NaOH溶液洗”需要用到的玻璃仪器是分液漏斗、烧杯.
(3)向“水洗”后所得水相中滴加KSCN溶液,溶液变红色.推测水洗的主要目的是除去FeBr3.
(4)锥形瓶中蒸馏水变黄的原因是溶解了从烧瓶中挥发出的溴.
(5)已知苯与溴发生的是取代反应,推测反应后锥形瓶中液体含有的两种大量离子,并设计实验方案验证你的推测.
(限选试剂:镁条、四氯化碳、氯水、溴水、蒸馏水)


反应剧烈进行,烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现,蒸馏水逐渐变成黄色.反应停止后按
如图2流程分离产品:
已知:溴苯难溶于水,与有机溶剂互溶;溴、苯、溴苯的沸点依次为59℃、80℃、156℃.
(1)操作Ⅰ为过滤,操作Ⅱ为蒸馏.
(2)“水洗”、“NaOH溶液洗”需要用到的玻璃仪器是分液漏斗、烧杯.
(3)向“水洗”后所得水相中滴加KSCN溶液,溶液变红色.推测水洗的主要目的是除去FeBr3.
(4)锥形瓶中蒸馏水变黄的原因是溶解了从烧瓶中挥发出的溴.
(5)已知苯与溴发生的是取代反应,推测反应后锥形瓶中液体含有的两种大量离子,并设计实验方案验证你的推测.
(限选试剂:镁条、四氯化碳、氯水、溴水、蒸馏水)
| 序号 | 实验步骤 | 预期现象 | 结论 |
| 1 | |||
| 2 | 锥形瓶中液体含大量Br- | ||
| 3 | 锥形瓶中液体含大量H+ |

3.相同质量的下列各烃,完全燃烧后生成CO2最多的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 乙烯 | D. | 苯 |
