题目内容
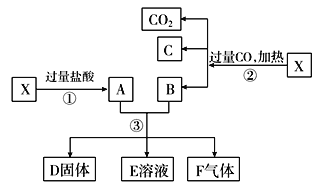
【题目】现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应条件没有标出)。
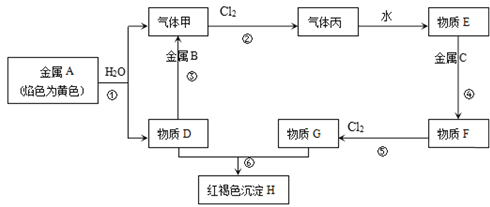
请回答下列问题:
(1)写出下列物质的化学式:B___、丙____;
(2)写出下列反应的离子方程式:
反应③_____;
反应⑤_____;
(3)向F的溶液中加入D溶液后产生的现象是____,用化学反应方程式解释产生此现象的原因____、___。
【答案】Al HCl 2Al+2OH-+2H2O=2AlO2-+3H2↑ 2Fe2++Cl2=2Fe3++2Clˉ 先变成白色沉淀,然后迅速变成灰绿色,最后变成红褐色沉淀 FeCl2+2NaOH=Fe(OH)2↓+2NaCl 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
金属A焰色反应为黄色证明为Na,与水反应生成气体甲为H2,D为NaOH;金属B和氢氧化钠溶液反应,说明B为Al,黄氯色气体乙为Cl2,气体甲和氯气反应生成丙为HCl,物质E为盐酸溶液,物质D氢氧化钠和物质G为反应生成红褐色沉淀H为Fe(OH)3,G为FeCl3,推断物质F为FeCl2;判断C为Fe。
(1)依据分析B为Al,E为HCl;
(2)反应③是氢氧化钠和铝反应生成氢气和偏铝酸钠,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑ ;
反应⑤是氯化亚铁和氯气反应生成氯化铁的反应,反应的化学方程式为:2FeCl2+Cl2=2FeCl3,离子方程式为:2Fe2++Cl2=2Fe3++2Clˉ ;
(3)F为FeCl2,D为NaOH,向F溶液中加入D溶液,生成氢氧化亚铁白色沉淀,在空气中被氧化成氢氧化铁,氢整个反应过程的实验现象是先有白色沉淀出现,然后白色沉淀逐渐变为墨绿色最终变为红褐色,涉及的化学方程式为:FeCl2+2NaOH=Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O═4Fe(OH)3。

 阅读快车系列答案
阅读快车系列答案【题目】已知25 ℃时部分弱电解质的电离平衡常数如下表所示:
化学式 | CH3COOH | H2CO3 | HClO | |
平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1 mol·L-1的四种溶液:
a. CH3COOH b. H2CO3 c. NaHCO3 d. HClO
pH由小到大的排列顺序是____(填字母)。
(2)常温下,0.1 mol·L-1CH3COOH溶液加水稀释过程中,下列表达式的数值变大的是____(填字母)。
A. c(H+) B.![]() C. c(H+)·c(OH-) D.
C. c(H+)·c(OH-) D.![]() E.
E.![]()
(3)体积均为100 mL、pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如下图所示,则HX的电离平衡常数____(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数,理由是____。在上述体积、pH均相同的CH3COOH与一元酸HX中加入足量的锌,生成的氢气在相同情况的体积大小关系为:CH3COOH____(填“大于”、“小于”或“等于”)HX