题目内容
已知X,Y,Z,Q为短周期非金属元素,R是长周期元素,X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍;Y的基态原子有7种不同运动状态的电子;Z元素在地壳中含量最多;Q是电负性最大的元素;R+离子只有三个电子层且完全充满电子。
回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
(1)X元素为???????? ,X、Y、Z中第一电离能最大的是???????? 。
(2)已知Y2Q2分子存在如图所示的两种结构(球棍模型,短线不一定代表单键):


该分子中Y原子的杂化方式是???????? 。
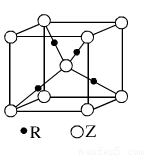
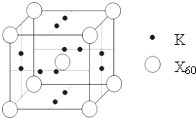
(3)X与Y元素可以形成一种超硬新材料,其晶体部分结构如图所示,有关该晶体的说法正确的是???? (填正确答案编号)。

A.该晶体属于分子晶体
B.此晶体的硬度比金刚石还大
C.晶体的化学式是X3Y4
D.晶体熔化时破坏共价键
(4)有一种AB型分子与Y单质分子互为等电子体,它是一种常用的还原剂,其化学式为????????????? 。
(5)R的基态原子的电子排布式为????????? ,R与Z形成的某离子晶体的晶胞结构如图,则该晶体的化学式为????????? ,该晶体的密度为a g·cm-3,则晶胞的体积是????????? cm3。
(1)C(1分)? N(1分)
(2)sp2(2分)
(3)bcd(3分)
(4)CO(2分)
(5)1s22s22p63s23p63d104s1或[Ar]3d104s1(2分)? Cu2O(2分)? 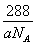 (2分)
(2分)
【解析】
试题分析:(1)X、Y、Z、Q为短周期非金属元素,R是长周期元素,X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍,且为非金属,则X为C元素;Y的基态原子有7种不同运动状态的电子,则Y为N元素;Z元素在地壳中含量最多,则Z为O元素;Q是电负性最大的元素,则Q为F元素;R+离子只有三个电子层且完全充满电子,则R为Cu元素.由分析可知:X为C元素;Y为N元素;Z为O元素;Q为F元素;R为Cu元素.
(2)杂化轨道数=σ键数+孤对电子对数,该分子中N原子的杂化轨道数=2+1=3,所以N原子杂化方式是sp2杂化,故答案为:sp2杂化;
(3)A、X与Y元素可以形成一种超硬新材料,由晶体部分结构可知,该晶体为原子晶体,故A错误;
B、C-N键键长比C-C键长短,C-N键键能大,所以晶体的硬度比金刚石还大,故B正确;
C、结构中每个X原子周围有4个Y原子,每个Y原子周围有3个X原子,所以该晶体化学式为X3Y4,即为C3N4,故C正确;
D、该晶体为原子晶体,晶体熔化时共价键被破坏,没有克服范德华力和氢键,故D正确.
故答案为:BCD。
(4)根据定义,原子数相同,电子总数相同的分子,互称为等电子体,所以与N2分子互为等电子体为CO。
(5)R为Cu元素,基态原子的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1;R与Z形成的某离子晶体的晶胞中铜原子的个数为体心4×1=4,氧原子个数为顶点8×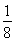 +体心1×1=2,所以该晶体的化学式为Cu2O;该晶体的密度为a g·cm-3,ρ=
+体心1×1=2,所以该晶体的化学式为Cu2O;该晶体的密度为a g·cm-3,ρ=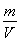 ;则晶胞的体积是a=
;则晶胞的体积是a= ;V=
;V= 。
。
考点:考查物质结构的综合知识。

 (2011?锦州模拟)【化学--物质结构与性质】
(2011?锦州模拟)【化学--物质结构与性质】 NH3?H2O+H+
NH3?H2O+H+ H++HO2-HO2-
H++HO2-HO2- H++O22-
H++O22-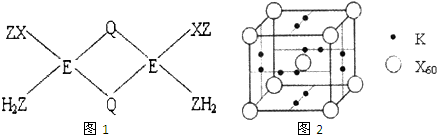 已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满.请回答下列问题:
已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满.请回答下列问题: 甲、乙可化合生成离子化合物丙。试回答下列问题:
甲、乙可化合生成离子化合物丙。试回答下列问题: