题目内容
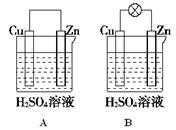
(16分)(1)把一块纯净的锌片插入盛有稀硫酸的烧杯里,可观察到锌片逐渐溶解,并有气体产生,再平行地插入一块铜片(如图甲所示),可观察到铜片上 (填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来(如图乙所示),可观察到铜片上(填“有”或“没有”) 气泡产生。
(2)用导线连接灵敏电流表的两端后,再与溶液中的锌片和铜片相连(如图丙所示),观察到灵敏电流表的指针发生了偏转,说明了导线中有电流通过。从上述现象中可以归纳出构成原电池的一些条件是 ,
有关的电极反应式:锌片 ;铜片 。
图丙所示原电池中,电子流向为 。
(3)图乙、图丙是一个将 能转化为 能的装置,人们把它叫做原电池。
(1)没有(2分),有(2分);
(2)两电极要插入电解质溶液,并用导线连接形成回路 (2分)
Zn-2e-=Zn2+(2分),2H+ + 2e- =H2↑(2分),从锌通过导线流向铜(2分)
(3)化学(2分),电能(2分)
解析

练习册系列答案
相关题目