题目内容
【题目】某学习小组用凯氏定氮法(Kjeldahl method)来测定农产品中氮的含量,测定过程如下:
I.用热浓硫酸处理0.25g谷物样品,把有机氮转化为铵盐。
II.用下图所示装置处理上述铵盐(夹持装置略去)。
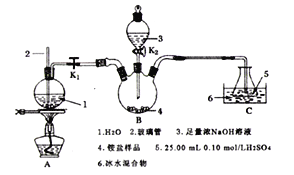
回答下列问题:
(1)实验前要检验B装置的气密性,具体操作为______________________________。
(2)盛放氢氧化钠溶液的仪器名称为__________________;玻璃管2的作用是___________________;圆底烧瓶中碎瓷片的作用是_________________________________________。
(3)将“谷物处理后所得的铵盐”加入三颈瓶中,打开玻璃塞、旋开K2,加入足量氢氧化钠溶液,关闭K2,打开K1,点燃酒精灯使水蒸气进入B装置。
①B装置中反应的离子方程式为_______________________________。
②C装置冰水混合物的作用是__________________________________。
III.滴定、计算氮的含量
(4)取下锥形瓶,加入指示剂,用0.10mol/L的NaOH溶液滴定,重复滴定3次,平均消耗19.30mLNaOH溶液。
①该滴定的指示剂应选择____________________。
a.甲基橙 b.配酞 c.甲基橙或酚酞
②该谷物样品中氮的百分含量为_____________。(保留2位小数)
【答案】 关闭K1、K2,锥形瓶中加水浸没导管,微热三颈烧瓶,锥形瓶内的导管口产生气泡,松手后,倒吸一段水柱,不下降,气密性良好 分液漏斗 避免b中压强过大 防止溶液暴沸 NH4++OH- ![]() NH3↑+H2O 降低温度,使氨气被充分吸收 a 17.20%或17.19%
NH3↑+H2O 降低温度,使氨气被充分吸收 a 17.20%或17.19%
【解析】(1)实验前要检验B装置的气密性,具体操作为:关闭K1、K2,锥形瓶中加水浸没导管,微热三颈烧瓶,锥形瓶内的导管口产生气泡,松手后,倒吸一段水柱,不下降,气密性良好;(2)氢氧化钠溶液盛放在分液漏斗中,玻璃管2用是起到平衡压强的作用,避免b中压强过大;烧瓶中碎瓷片的作用是防止溶液暴沸。(3)①B装置中反应的离子方程式为:NH4++OH- ![]() NH3↑+H2O ;②C装置冰水混合物可以降低温度,使氨气被充分吸收;(4)用强碱滴定酸,故用甲基橙作指示剂,选a;②n(NH3)+n(OH-)=n(H+),代入数据可得n(NH3)=0.00307mol,该谷物样品中氮的百分含量为0.00307mol ×14g/mol/0.25g==17.19%。
NH3↑+H2O ;②C装置冰水混合物可以降低温度,使氨气被充分吸收;(4)用强碱滴定酸,故用甲基橙作指示剂,选a;②n(NH3)+n(OH-)=n(H+),代入数据可得n(NH3)=0.00307mol,该谷物样品中氮的百分含量为0.00307mol ×14g/mol/0.25g==17.19%。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案