题目内容
【题目】2019年诺贝尔化学奖颁给在锂离子电池发展方面作出突出贡献的三位科学家,颁奖词中说:他们创造了一个可再充电的世界。下面是最近研发的Ca-LiFePO4可充电电池的工作示意图,锂离子导体膜只允许Li+通过,电池反应为:xCa2++2LiFePO4![]() xCa+2Li1-xFePO4+2xLi+。下列说法错误的是
xCa+2Li1-xFePO4+2xLi+。下列说法错误的是
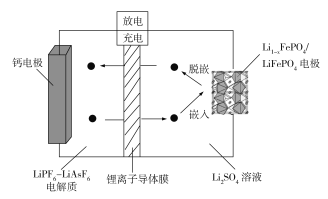
A.LiPF6-LiAsF6为非水电解质,其与Li2SO4溶液的主要作用都是传递离子
B.放电时,负极反应为:LiFePO4xe===Li1-xFePO4+xLi+
C.充电时,Li1-xFePO4/LiFePO4电极发生Li+脱嵌,放电时发生Li+嵌入
D.充电时,当转移0.2 mol电子时,左室中电解质的质量减轻2.6 g
【答案】B
【解析】
钙与水能够剧烈反应,所以,左室中的LiPF6LiAsF6电解质一定为非水电解质,Li2SO4溶液为右室中的电解质溶液,它们的主要作用都是传递离子,形成电流,构成闭合回路,A正确;放电时,负极反应为:Ca2e===Ca2+,使左室中正电荷数目增多,锂离子导体膜只允许Li+通过,使LiPF6LiAsF6电解质中的Li+通过锂离子导体膜移入右室,正极反应为:Li1xFePO4+xLi++xe===LiFePO4,电极发生Li+嵌入,B错误;充电时,阳极发生:LiFePO4xe===xLi++Li1xFePO4,电极发生Li+脱嵌,阴极发生:Ca2++2e===Ca,转移0.2 mol电子时,有0.2 mol Li+从右室通过锂离子导体膜移入左室,左室电解质中有0.1 mol Ca2+得电子生成Ca沉积在钙电极上,故左室中电解质的质量减轻40×0.1 g 7×0.2 g =2.6 g,C、D正确。

【题目】化学反应速率和化学反应的限度是化学反应原理的重要组成部分。
(1)探究反应条件对0.10mol/LNa2S2O3溶液与0.10mol/L 稀H2SO4反应速率的影响。反应方程式为:Na2S2O3 +H2SO4=Na2SO4+S↓+SO2↑+H2O。设计测定结果如下:
编号 | 反应温度/℃ | Na2S2O3溶液/mL | 甲/mL | H2SO4溶液/mL | 乙 |
① | 25 | 10.0 | 0 | 10.0 | x |
② | 25 | 5.0 | A | 10.0 | y |
③ | 0 | 10.0 | 0 | 10.0 | z |
若上述实验①②是探究浓度对化学反应速率的影响,则a为____________,乙是实验需要测量的物理量,则表格中“乙”为____________,x、y、z的大小关系是____________。
(2)氨气具有广泛的用途,工业上合成氨的反应是N2(g)+3H2(g)=2NH3(g).
①已知:
化学键 | H-H | N≡N | N-H |
键能kJ/mol(断开1mol化学键所需要的能量) | 436 | 945 | 391 |
则合成氨的热化学方程式是________________________________________。
②若反应起始时N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.1mol/L,达到平衡时NH3浓度的范围是____________________。
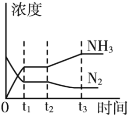
③如图表示该反应在t1时刻达到化学平衡,在t2时因改变某个条件而发生变化的情况,则t2时刻改变条件可能是__________。