题目内容
19.向25mL 2mol•L-1的稀硫酸中加入25mL 1mol•L-1的BaCl2溶液,充分反应后,溶液中H+物质的量浓度为(溶液混后体积变化忽略不计)( )| A. | 2mol•L-1 | B. | 1mol•L-1 | C. | 0.5mol•L-1 | D. | 0.25mol•L-1 |
分析 稀硫酸中进入氯化钡溶液后,反应生成硫酸钡沉淀和HCl,溶液中氢离子的物质的量不变,根据n=cV计算出硫酸的物质的量及含有的氢离子的物质的量,再根据混合液体积计算出混合液中氢离子的物质的量浓度.
解答 解:25mL 2mol•L-1的稀硫酸中含有硫酸的物质的量为:2mol/L×0.025L=0.05mol,含有氢离子的物质的量为:0.05mol×2=0.1mol,
向该稀硫酸溶液中加入氯化钡溶液后,氢离子的物质的量不变,溶液体积变为50mL,
则混合液中氢离子的物质的量浓度为:$\frac{0.1mol}{0.05L}$=2mol/L,
故选A.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确加入氯化钡溶液后发生反应的实质为解答关键,注意掌握物质的量浓度的概念及计算方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
7.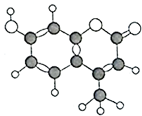 某种有机物由C、H、O三种元素组成,其分子球棍模型如图所示,下列有关叙述正确的是( )
某种有机物由C、H、O三种元素组成,其分子球棍模型如图所示,下列有关叙述正确的是( )
①分子式为C10H9O3
②该分子中10个碳原子都可能在同一平面上
③1mol该物质最多能与5molH2加成
④该物质能使酸性KMnO4溶液褪色
⑤1mol该物质最多能与含3molNaOH的溶液反应
⑥1mol该物质与足量浓溴水反应,最多消耗3molBr2
⑦该物质遇FeCl2溶液不变色
⑧该物质能和Na2CO3溶液、NaHCO3溶液反应.
 某种有机物由C、H、O三种元素组成,其分子球棍模型如图所示,下列有关叙述正确的是( )
某种有机物由C、H、O三种元素组成,其分子球棍模型如图所示,下列有关叙述正确的是( )①分子式为C10H9O3
②该分子中10个碳原子都可能在同一平面上
③1mol该物质最多能与5molH2加成
④该物质能使酸性KMnO4溶液褪色
⑤1mol该物质最多能与含3molNaOH的溶液反应
⑥1mol该物质与足量浓溴水反应,最多消耗3molBr2
⑦该物质遇FeCl2溶液不变色
⑧该物质能和Na2CO3溶液、NaHCO3溶液反应.
| A. | ①②④⑥ | B. | ②③⑤⑥ | C. | ②④⑦⑧ | D. | ②④⑤⑥ |
4.在A+B(s)?C的反应中,若增大压强或降低温度,B的转化率均增大,则反应体系应是( )
| A. | A是固体,C是气体,正反应吸热 | B. | A是气体,C是液体,正反应放热 | ||
| C. | A是气体,C是气体,正反应放热 | D. | A是气体,C是气体,正反应吸热 |
11.某离子的原子核里有n个质子,该离子的电子层排布与氩原子相同,它所带的电荷可能是( )
| A. | +(n-18) | B. | -n | C. | -(n+18) | D. | +(18-n) |
16.下列离子方程式正确的是( )
| A. | FeBr2溶液中通入少量的Cl2:Cl2+2Fe2+═2Fe3++2Cl- | |
| B. | 大理石溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 向NaHSO4溶液中滴加Ba(OH)2至刚好沉淀完全:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | NaOH溶液中通入过量SO2气体:SO2+2OH-═SO32-+H2O |
 除氢元素外,非金属元素都在p区,d区元素全部是金属.
除氢元素外,非金属元素都在p区,d区元素全部是金属. .
.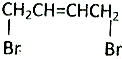 可经四步反应制取HOOCCH=CHCOOH.
可经四步反应制取HOOCCH=CHCOOH.