��Ŀ����
����Ŀ�������ӹ���ķ�����Һ�к�2%��3%��NaNO2������һ�ֻ�����Ⱦ�������NH4Cl��Һ������������Һ��ʹNaNO2ת��Ϊ�����ʣ��÷�Ӧ���������У�
��һ����NaNO2+NH4Cl=NaCl+NH4NO2
�ڶ�����NH4NO2=N2��+2H2O
���жԵڶ�����Ӧ����������ȷ����
��NH4NO2ֻ�������� ��NH4NO2ֻ�ǻ�ԭ��
��NH4NO2�����˷ֽⷴӦ ��ֻ�е�Ԫ�صĻ��ϼ۷����˱仯
��NH4NO2�������������ǻ�ԭ��
A. �٢� B. �٢� C. �ڢۢ� D. �ۢܢ�
���𰸡�D
�����������⿼��������ԭ��Ӧ�Ļ�������ڶ�����Ӧ��NH4NO2������������������ԭ��Ӧ�����е�Ԫ�ط����˹��з�Ӧ��NH4NO2�������������ǻ�ԭ�������Ĵ������Ӧ���Ϳ���NH4NO2�������ǷֽⷴӦ�������ۢܢ�����ȷ�ġ���Dѡ��������⡣
�����͡���ѡ��
��������
16
����Ŀ����ͼ��ʾAlCl3��Һ��NaOH��Һ��μӻ�ϣ���ͼ���жϴ�����ǣ� ��
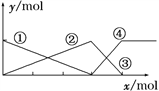
A. ���߱�ʾAl3+���ʵ����ı仯
B. x��ʾAlCl3�����ʵ���
C. ���߱�ʾAl(OH)3���ʵ����ı仯
D. ���߱�ʾAlO![]() ���ʵ����ı仯
���ʵ����ı仯
���𰸡�B
���������ٶ�����1molAlCl3��Һ�еμ�NaOH��Һ�����ȷ�����ӦAl3++3OH-=Al(OH)3����Al3+��ȫ����������3molOH-������1molAl(OH)3��Ȼ������ӦAl(OH)3+OH-=AlO2-+2H2O��������ȫ�ܽ�����1molOH-������1molAlO2-��ǰ�����������ĵ�OH-Ϊ3��1���ٶ�����4molNaOH��Һ�еμ�AlCl3��Һ�����ȷ�����ӦAl3++4OH-=AlO2-+2H2O��OH-��ȫ��Ӧ����1molAl3+������1molAlO2-��Ȼ������ӦAl3++3AlO2-+6H2O=4Al(OH)3����AlO2-��ȫ��Ӧ������![]() molAl3+������
molAl3+������![]() molAl(OH)3����ǰ�����������ĵ�Al3+Ϊ1mol��
molAl(OH)3����ǰ�����������ĵ�Al3+Ϊ1mol�� ![]() mol=3��1����ͼ���֪���٢ڱ�ʾ�����ܱۢ�ʾ�����ʵ�����ϵΪ1��1��֪����ͼ��ʾ��AlCl3��Һ�еμ�NaOH��Һ��A��������������֪�����ȷ�����ӦAl3++3OH-=Al(OH)3������Һ�����������ʵ������٣����߱�ʾAl3+�����ʵ����ı仯��ѡ��A��ȷ��B��������������֪��x��ʾNaOH��Һ��ѡ��B����C��������������֪���淴Ӧ����Al(OH)3���ʵ��������������С���ʢڢ��߱�ʾAl(OH)3�����ʵ����ı仯��ѡ��C��ȷ��D��������������֪��Al(OH)3�ܽ�ʱ��AlO2-�����ʵ��������߱�ʾAlO2-�����ʵ����ı仯��ѡ��D��ȷ����ѡB��
mol=3��1����ͼ���֪���٢ڱ�ʾ�����ܱۢ�ʾ�����ʵ�����ϵΪ1��1��֪����ͼ��ʾ��AlCl3��Һ�еμ�NaOH��Һ��A��������������֪�����ȷ�����ӦAl3++3OH-=Al(OH)3������Һ�����������ʵ������٣����߱�ʾAl3+�����ʵ����ı仯��ѡ��A��ȷ��B��������������֪��x��ʾNaOH��Һ��ѡ��B����C��������������֪���淴Ӧ����Al(OH)3���ʵ��������������С���ʢڢ��߱�ʾAl(OH)3�����ʵ����ı仯��ѡ��C��ȷ��D��������������֪��Al(OH)3�ܽ�ʱ��AlO2-�����ʵ��������߱�ʾAlO2-�����ʵ����ı仯��ѡ��D��ȷ����ѡB��