题目内容
【题目】已知:25℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10mL0.1mol·L-1醋酸溶液测得其pH=3。0.1mol·L-1氨水(NH3·H2O溶液)的pH=___。用pH试纸测定该氨水pH的操作方法为_____。氨水(NH3·H2O溶液)电离平衡常数表达式Kb=____,25℃时,氨水电离平衡常数约为_____。
(2)25℃时,现向10mL0.1mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中![]() ___(填序号)。
___(填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
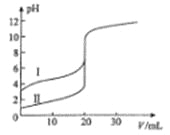
(3)某温度下,向V1mL0.1mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=-lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是____(填字母,下同)。图中M、Q、N三点所示溶液中水的电离程度最大的点是____。
【答案】11 取一小段pH试纸放在表面皿上,用洁净的玻璃棒蘸取氨水溶液滴在pH试纸上,然后与标准比色卡对照读取pH值 ![]() 10-5 b Q Q
10-5 b Q Q
【解析】
(1)醋酸的电离平衡常数等于NH3·H2O的电离平衡常数,因此氨水中c(OH-)=10-3mol·L-1,根据水的离子积,c(H+)=Kw/c(OH-)=10-14/10-3=10-11mol·L-1,因此pH=11,取一小段pH试纸放在表面皿上,用洁净的玻璃棒蘸取氨水溶液滴在pH试纸上,然后与标准比色卡对照读取pH值;③根据电离平衡常数的定义,因此Kb=![]() ,弱电解质的电离微弱,NH3·H2O的浓度仍为0.1mol·L-1,Kb=10-310-3/0.1=10-5。故答案为:11;取一小段pH试纸放在表面皿上,用洁净的玻璃棒蘸取氨水溶液滴在pH试纸上,然后与标准比色卡对照读取pH值;
,弱电解质的电离微弱,NH3·H2O的浓度仍为0.1mol·L-1,Kb=10-310-3/0.1=10-5。故答案为:11;取一小段pH试纸放在表面皿上,用洁净的玻璃棒蘸取氨水溶液滴在pH试纸上,然后与标准比色卡对照读取pH值;![]() ;10-5;
;10-5;
(2)NH3·H2O![]() NH4++OH-,加入醋酸,消耗OH-,促进电离,n(NH4+)增加,n(NH3·H2O)降低,比值增大,故选项b正确。
NH4++OH-,加入醋酸,消耗OH-,促进电离,n(NH4+)增加,n(NH3·H2O)降低,比值增大,故选项b正确。
(3)溶液显中性,即c(OH-)=c(H+),即Q点,酸和碱抑制水的电离,随着反应进行,碱性减弱,对水电离抑制减弱,恰好反应,生成醋酸钠,发生盐类水解,促进水的电离,然后随着醋酸的增多,对水的抑制增加,因此水电离程度最大的是Q点。故答案为Q,Q。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案