题目内容
能正确表示下列化学反应的离子方程式是( )A.将0.5 mol Cl2通入含1 mol FeBr2的溶液中:2Cl2+2Fe2++2Br-====2Fe3++Br2+4Cl-
B.碳酸氢铵与热的浓NaOH溶液反应:![]() +OH-====NH3↑+H2O
+OH-====NH3↑+H2O
C.在漂白粉溶液中通入过量二氧化碳:ClO-+CO2+H2O====HClO+![]()
D.将物质的量浓度相同的NaHCO3溶液和Ba(OH)2溶液等体积混合:
![]() +Ba2++OH-====BaCO3↓+H2O
+Ba2++OH-====BaCO3↓+H2O
CD
解析:A项中由于考虑氧化性顺序Cl2>Br2>Fe3+,Cl2先与Fe2+反应,再与Br-反应,本题中0.5 mol Cl2与1 mol Fe2+恰好反应,正确的离子方程式为:Cl2+2Fe2+====2Fe3++2Cl-;B项中忽略了![]() 与OH-作用,应写成:
与OH-作用,应写成:![]() +
+![]() +2OH-====NH3↑+
+2OH-====NH3↑+![]() +2H2O;C、D项均正确。
+2H2O;C、D项均正确。

练习册系列答案
相关题目
在下列各说法中,正确的是( )
| A、对于2SO2(g)+O2(g)?2SO3(g)△H=-QkJ?mol-1,(Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量一定是Q/2 kJ | B、热化学方程式中的化学计量数不能用分数表示 | C、Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0,该反应的化学能可以转化为电能 | D、△H的大小与热化学方程式的化学计量数无关 |
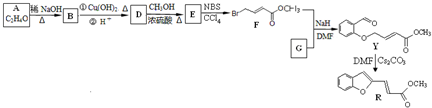
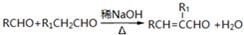 (R、R1表示烃基或氢)
(R、R1表示烃基或氢)
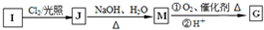


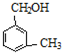 互为同系物
互为同系物