题目内容
 (2011?上海)实验室制取少量溴乙烷的装置如右图所示.根据题意完成下列填空:
(2011?上海)实验室制取少量溴乙烷的装置如右图所示.根据题意完成下列填空:(1)圆底烧瓶中加入的反应物是溴化钠、
乙醇
乙醇
和1:1的硫酸.配制体积比1:1的硫酸所用的定量仪器为b
b
(选填编号).a.天平 b.量筒 c.容量瓶 d.滴定管
(2)写出加热时烧瓶中发生的主要反应的化学方程式
NaBr+H2SO4═HBr+NaHSO4、HBr+CH3CH2OH
CH3CH2Br+H2O
| 加热 |
NaBr+H2SO4═HBr+NaHSO4、HBr+CH3CH2OH
CH3CH2Br+H2O
.| 加热 |
(3)将生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是
冷却、液封溴乙烷
冷却、液封溴乙烷
.试管A中的物质分为三层(如图所示),产物在第
3
3
层.(4)试管A中除了产物和水之外,还可能存在
HBr
HBr
、CH3CH2OH
CH3CH2OH
(写出化学式).(5)用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是
d
d
(选填编号).a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称是
乙烯
乙烯
.(6)实验员老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:
反应会产生Br2,腐蚀橡胶
反应会产生Br2,腐蚀橡胶
.分析:(1)从制取的目标物质以及有机物的性质角度,结合质量守恒定律来分析,根据仪器的使用方法和实验的目的来选择所需仪器;
(2)根据物质的性质来书写化学方程式;
(3)根据实验仪器的特点和有机物的性质来分析;
(4)根据反应物的性质来分析;
(5)根据反应物的性质来分析;
(6)根据溴的性质分析.
(2)根据物质的性质来书写化学方程式;
(3)根据实验仪器的特点和有机物的性质来分析;
(4)根据反应物的性质来分析;
(5)根据反应物的性质来分析;
(6)根据溴的性质分析.
解答:解:(1)实验室制取少量溴乙烷所用试剂是乙醇和溴化氢反应,二者在加热下发生取代反应生成溴乙烷;此实验量取溶液的体积要求精确度不是很高,可用量筒量取,故答案为:乙醇; b;
(2)药品混合后在加热条件下生成HBr并和乙醇发生取代反应,故答案为:NaBr+H2SO4═HBr+NaHSO4、HBr+CH3CH2OH
CH3CH2Br+H2O;
(3)收集装置所用导气管较长,可以起到冷却的作用,生成的溴乙烷和水互不相溶,并且溴乙烷的密度比水大,在冰水混合物的下层,故答案为:冷却、液封溴乙烷; 3;
(4)在加热条件下反应,HBr和CH3CH2OH都易挥发,故生成物中有存在HBr、CH3CH2OH,故答案为:HBr;CH3CH2OH;
(5)试管A中获得的有机物呈棕黄色,是由于浓硫酸具有强氧化性,将HBr氧化物Br2,产物为溴乙烷,混有单质溴,蒸馏不能完全除去杂质,并且操作麻烦,氢氧化钠溶液易使溴乙烷水解,四氯化碳会引入新的杂质,而亚硫酸钠和溴发生氧化还原反应生成HBr和硫酸钠,易与溴乙烷分离.,在加热温度较高时,乙醇发生消去反应生成乙烯,
故答案为:d; 乙烯;
(6)浓硫酸具有强氧化性,将HBr氧化物Br2,生成的Br2具有强氧化性,会腐蚀橡胶,应用玻璃导管,故答案为:反应会产生Br2,腐蚀橡胶;
(2)药品混合后在加热条件下生成HBr并和乙醇发生取代反应,故答案为:NaBr+H2SO4═HBr+NaHSO4、HBr+CH3CH2OH
| 加热 |
(3)收集装置所用导气管较长,可以起到冷却的作用,生成的溴乙烷和水互不相溶,并且溴乙烷的密度比水大,在冰水混合物的下层,故答案为:冷却、液封溴乙烷; 3;
(4)在加热条件下反应,HBr和CH3CH2OH都易挥发,故生成物中有存在HBr、CH3CH2OH,故答案为:HBr;CH3CH2OH;
(5)试管A中获得的有机物呈棕黄色,是由于浓硫酸具有强氧化性,将HBr氧化物Br2,产物为溴乙烷,混有单质溴,蒸馏不能完全除去杂质,并且操作麻烦,氢氧化钠溶液易使溴乙烷水解,四氯化碳会引入新的杂质,而亚硫酸钠和溴发生氧化还原反应生成HBr和硫酸钠,易与溴乙烷分离.,在加热温度较高时,乙醇发生消去反应生成乙烯,
故答案为:d; 乙烯;
(6)浓硫酸具有强氧化性,将HBr氧化物Br2,生成的Br2具有强氧化性,会腐蚀橡胶,应用玻璃导管,故答案为:反应会产生Br2,腐蚀橡胶;
点评:本题主要考察溴乙烷大制备、提纯、有机反应等复杂性以及实验安全等.第1、2、3问,源于课本中对该演示实验的实验报告,特别是第6问中“标准玻璃接口”这一装置,如果没有认真研究过教材,就不会很熟悉该装置.建议同学们精心选择一些取之于教材,但又高于教材的习题.这类题的答案就在教材之中,若不重视教材就很难取得好成绩.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目

 (2011?上海)如图是实验室制取HCl气体NaCl+H2SO4(浓)
(2011?上海)如图是实验室制取HCl气体NaCl+H2SO4(浓)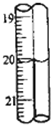 第2次滴定后滴定管的读数如图所示,将这一读数填入上表中.根据表中的数据计算出盐酸的浓度为
第2次滴定后滴定管的读数如图所示,将这一读数填入上表中.根据表中的数据计算出盐酸的浓度为