题目内容
|
某温度下在密闭容器中发生如下反应: 2M(g)+N(g) 若开始时只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2 mol M和1 mol N的混合气体,达平衡时M的转化率为 | |
| [ ] | |
A. |
20% |
B. |
40% |
C. |
60% |
D. |
80% |
答案:C
解析:
解析:
|
“某温度下混合气体的压强比起始时增大了”,言外之意是容积不变.由下图可知,开始时只充入2 mol E(g)和开始时只充入2 mol M和1 mol N的混合气体相比,达到的化学平衡完全相同(等效平衡).
在Ⅰ中,达平衡时混合气体的压强比起始时增大了20%,也就是气体的物质的量增加了20%,此时混合气体的总物质的量是2.4 mol.Ⅱ和Ⅰ之间具有等效平衡关系,则Ⅱ中达到化学平衡时混合气体的总物质的量也是2.4 mol,比开始时减少了0.6 mol.设M的平衡转化值为x.
点拨:该题还可以分别采用下列两种解法. |

练习册系列答案
相关题目
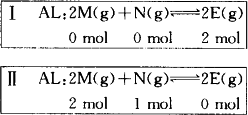
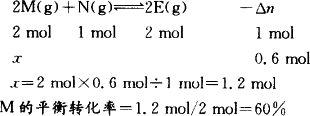

 2E(g),若开始时只充入2 mol
E气体,达平衡时,混合气体的压强比起始增大了20%;若开始时只充入3 molM和1 mol N的混合气体,达到平衡时M的转化率为
2E(g),若开始时只充入2 mol
E气体,达平衡时,混合气体的压强比起始增大了20%;若开始时只充入3 molM和1 mol N的混合气体,达到平衡时M的转化率为