题目内容
(8分)铁是人类较早使用的金属之一,根据所学铁及其化合物的知识,回答下列问题:
(1)下列各物质中,不能和单质铝反应的物质是 (填下列各项序号)。
①Fe ②FeCl3 ③FeSO4
(2)向沸水中逐滴滴加1mol·L-1FeCl3溶液,至液体呈透明的红褐色,实验得到的分散系
属于 (填“溶液”“浊液”或“胶体”),所得到的分散系中的分散质具有的性质有如下的 (填写序号)。
①电泳 ②透过半透膜 ③聚沉 ④具有强还原性
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的化学方程式: ;证明反应后的溶液中存在Fe3+的实验方法是 。
(1)下列各物质中,不能和单质铝反应的物质是 (填下列各项序号)。
①Fe ②FeCl3 ③FeSO4
(2)向沸水中逐滴滴加1mol·L-1FeCl3溶液,至液体呈透明的红褐色,实验得到的分散系
属于 (填“溶液”“浊液”或“胶体”),所得到的分散系中的分散质具有的性质有如下的 (填写序号)。
①电泳 ②透过半透膜 ③聚沉 ④具有强还原性
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的化学方程式: ;证明反应后的溶液中存在Fe3+的实验方法是 。
(共8分) (1) (1分)① (2) (3分)胶体(1分)①③(2分)
(3) (4分)2FeCl3 + Cu = 2FeCl2 + CuCl2(2分);取试样少许滴入硫氰酸钾溶液,溶液显红色,证明溶液中含有Fe3+(2分)(其它答案合理则同样得分)
(3) (4分)2FeCl3 + Cu = 2FeCl2 + CuCl2(2分);取试样少许滴入硫氰酸钾溶液,溶液显红色,证明溶液中含有Fe3+(2分)(其它答案合理则同样得分)
试题分析:(1)铝是活泼的金属,且金属性强于铁的,所以铝能和氯化铁,以及氯化亚铁都反应,铁和铝不反应,答案选①。
(2)向沸水中逐滴滴加1mol·L-1FeCl3溶液,至液体呈透明的红褐色,所得到的分散系是胶体,胶体具有电泳现象、能发生聚沉,但氢氧化铁胶体不能透过半透膜、没有强还原性,答案选①③。
(3)氯化铁能和铜反应,生成氯化铜和氯化亚铁,反应的化学方程式是2FeCl3 + Cu = 2FeCl2 + CuCl2。检验铁离子常用试剂是KSCN溶液,即取试样少许滴入硫氰酸钾溶液,溶液显红色,证明溶液中含有Fe3+。
点评:该题是高考中的常见题型,所以注重基础性知识的考查,同时兼顾考查学生分析问题、解决问题的能力。有助于培养学生的逻辑思维能力和发散思维能力,以及严格的规范答题能力。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下: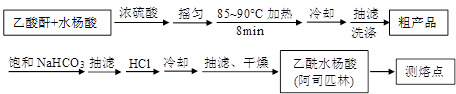
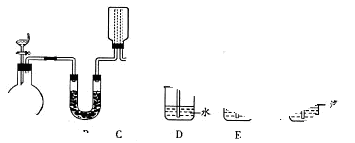
 改进的提纯方法中加热回流的装置如图所示
改进的提纯方法中加热回流的装置如图所示