��Ŀ����
����Ŀ������ѧ������ѧ�뼼�����������ƿ������ڸ��Ƶر�ˮ�ʡ��������ؽ������ӷ�ˮ�������ೱ��Ҳ������Ӧ�������ȡ�ʵ���ҿ��ù�ҵ̼���(��MgCO3��FeCO3������)��ȡ������̼��ƣ�Ȼ�����ô���̼�����ȡ�������ƣ�����Ҫ�������£�
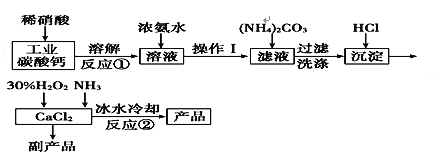
��֪��CaO2��8H2O�ʰ�ɫ����ˮ��������350�����ҿ�ʼ�ֽ�ų�������425���ֽ���ȫ��
��1��д����Ӧ����������ԭ��Ӧ�����ӷ���ʽ��___________________________��
��2����Ӧ�������Һ�м�Ũ��ˮ��Ŀ���ǣ�___________��________(�÷���ʽ��ʾ)
��3����Ӧ�����ñ�ˮ�����¶���0�����ң������ԭ����(д������)��
��__________________________����__________________________��
��4���ⶨ��Ʒ��CaO2�ĺ�����ʵ�鲽����
��һ����ȷ��ȡa g��Ʒ��������ƿ�У�������������ˮ������b g KI���壬�ٵ�������2 mol/L��H2SO4��Һ����ַ�Ӧ��
�ڶ�������������ƿ�м��뼸�ε�����Һ��
����������μ���Ũ��Ϊc mol��L��1��Na2S2O3��Һ����Ӧ��ȫ������Na2S2O3��ҺV mL����֪��I2��2S2O===2I����S4O��
ijͬѧ��һ���͵ڶ����IJ������ܹ淶������������̫����������õ�CaO2��������������________(�����Ӱ�족��ƫ�͡���ƫ�ߡ�)��ԭ����____________________.
���𰸡�(����ע3�����������2��) ��1��3FeCO3��10H����NO===3Fe3����NO����3CO2����5H2O(3��)
��2��Mg2��+��Fe3��������ȫ(����ʽ��) ��3������ֹH2O2�ֽ⣬�����������
������CaO2��8H2O�ܽ�ȣ���߲��� ��4��ƫ�� �����������¿����е�O2Ҳ����KI����ΪI2��ʹ���ĵ�Na2S2O3���࣬�Ӷ�ʹ��õ�CaO2����������ƫ��
��������
�����������1����Ӧ����ֻ��FeCO3�����ᷴӦ��������ԭ��Ӧ������������һ��������������̼��ˮ����Ӧ����ʽΪ��3FeCO3+10H++NO3-=3Fe3++NO��+3CO2��+5H2O��
��2�����백ˮʹMg2+��Fe3+������ȫ����Ӧ�����ӷ���ʽΪ��Mg2++2NH3H2O=Mg(OH)2��+2NH4+�� Fe3++3NH3H2O=Fe(OH)3��+3NH4+��
��3��H2O2�����ֽ⣬���ñ�ˮ�����¶���0�����ң���ֹ��ֽ⣬��������ʣ�ͬʱ�¶ȵ��ܽ���CaO28H2O�ܽ�ȣ���߲�����
��4��ijͬѧ��һ���͵ڶ����IJ������ܹ淶������������̫����������õ�CaO2��������������ƫ�ߣ���Ϊ�����������¿����е�O2Ҳ����KI����ΪI2��ʹ���ĵ�Na2S2O3���࣬�Ӷ�ʹ��õ�CaO2����������ƫ����

 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д�����Ŀ��A��B��C����ǿ����ʣ�������ˮ�е�������������±���ʾ��
������ | Na����K����Cu2�� |
������ | SO��OH�� |
����ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��������A��Һ��������B��Һ��������C��Һ���缫��Ϊʯī�缫��

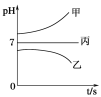
��ͨ��Դ������һ��ʱ�������ձ���c�缫����������16 g�������¸��ձ�����Һ��pH����ʱ��t�Ĺ�ϵ����ͼ���ݴ˻ش��������⣺
��1��MΪ��Դ��_____��(���������)���缫b�Ϸ����ĵ缫��ӦΪ__________________��
��2���缫e�����ɵ������ڱ�״̬�µ����Ϊ________��
��3��д�����ձ��еĵ��ط�Ӧ_______________________��
��4��Ҫʹ���ձ��е�C��Һ�ָ���ԭ����״̬����ȷ�IJ���__________�������������ݣ���