题目内容
羰基硫(OCS)是一种有臭鸡蛋气味的无色气体,分子结构与CO2相似,高温下分解为CO和S。下列有关说法正确的是( )
| A.OCS、CO2、CO、S晶体类型相同 |
| B.OCS高温分解时,碳元素化合价升高 |
| C.OCS中含有1个σ键和1个π键 |
| D.22.4 L OCS中约含有3×6.02× 1023个原子 |
A
解析试题分析:A.OCS、CO2、CO、S晶体类型相同,都是分子晶体,正确;B.在OCS中C的化合价是+4价,在高温分解时,产生CO,碳元素化合价变为+2价,化合价降低,错误;C.在OCS中含有2个σ键和2个π键,错误;D.22.4 L OCS气体由于气体的条件不知道,所以不能确定其物质的量的多少,因此分子中含有原子个数不能确定,错误。
考点:考查羰基硫的结构与性质的关系的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法中正确的是( )
| A.分子中键能越大,键长越长,则分子越稳定 |
| B.sp3杂化轨道是由同一个原子中能量相近的s 轨道和p轨道混合起来形成的一组能量相近的新轨道 |
| C.PCl5分子中P原子和Cl原子最外层都满足8电子结构 |
| D.用价层电子互斥理论预测H2S和BF3的立体结构,分别为V形和平面正三角形 |
下列物质的性质与氢键无关的是
| A.冰的密度比液态水的密度小 |
| B.NH3易液化 |
| C.在相同条件下,H2O的沸点比H2S的沸点高 |
| D.HF分子比HCl分子稳定 |
键能是指破坏(或形成)1mol化学键所吸收(或放出)的能量。现查得:H-H、Cl-Cl和H-Cl的键能分别为436KJ/mol、243KJ/mol和431KJ/mol,请用此数据估计,由Cl2、H2生成1molHCl时的热效应为
| A.放热91.5KJ | B.放热183KJ | C.吸热183KJ | D.吸热91.5KJ |
下列物质中含有共价键的离子化合物是( )
| A.Ba(OH)2 | B.CaCl2 | C.H2O | D.H2 |
下列说法正确的是
| A.熔化干冰和熔化NaCl晶体所克服的作用力相同 |
| B.氢键比分子间作用力强,所以它属于化学键 |
| C.H2O是一种非常稳定的化合物,这是由于氢键所致 |
| D.冰的密度比水小,这是由于冰中存在氢键所致 |
下列有关叙述正确的是
| A.氢键是一种特殊化学键,它广泛地存在于自然界中 |
| B.在CH3—CHOH—COOH分子中含有1个手性C原子 |
| C.碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子 |
| D.含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大 |
X、Y代表两组概念,其关系如下图,下列选项不满足相应关系的是 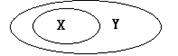
| 选项 | X | Y |
| A. | 氢键 | 化学键 |
| B. | SO2 | 漂白性物质 |
| C. | 油脂 | 酯 |
| D. | 置换反应 | 氧化还原反应 |