��Ŀ����
14�� ���������һ�����ͷ��ȸ�Ч�������������ڹ�ҵ��ˮ�����������ˮ�Ĵ�����ijС��ͬѧΪ�о�������ض�ˮ��Һ�б��ӵĽ��ⷴӦ���ʣ��ں㶨ʵ���¶�298K��318K�����£�����ʵ���������±�����������¶Ա�ʵ�飮
���������һ�����ͷ��ȸ�Ч�������������ڹ�ҵ��ˮ�����������ˮ�Ĵ�����ijС��ͬѧΪ�о�������ض�ˮ��Һ�б��ӵĽ��ⷴӦ���ʣ��ں㶨ʵ���¶�298K��318K�����£�����ʵ���������±�����������¶Ա�ʵ�飮��1�����������ʵ����Ʊ���
| ʵ���� | pH | Ͷ�ϱȣ���������뱽�ӵ������ȣ� | T/K | Fe3+ | ʵ��Ŀ�� |
| �� | 4 | 10��1 | 298 | 0 | ����ʵ�� |
| �� | 4 | 8��1 | 298 | 0 | |
| �� | ̽���¶ȶԸý��ⷴӦ���ʵ�Ӱ�� |
��3��ijͬѧ��ʵ���Ϊ����ʵ�飬��������ʵ��ͨ��HPLC����ò�ͬpH�¸�����ض�ˮ��Һ�б��ӵ�ȥ���ʣ�������ͼ��ʾ��
�ٹ�ҵ��ʹ�ø�����س�ȥ��ˮ�еı���ʱ��pH������2.5���ң�
������ͼ����Ϣ������һ��ʹ��Ӧֹͣ�ķ�������ӦҺ�м������ᣬʹ��ҺpH��2��
���� ��1������ʵ����Ʊ���֪��ʵ����̽��Ͷ�ϱȲ�ͬ������������ͬ���Ӷ�ȷ��ʵ��Ŀ�ģ������������䣬�ı��¶ȣ���Ӧ���ʸı䣻
��2��������ʵ�������иı�pH��ʵ�顢��Fe3+��ʵ�飻
��3���ٸ���ȥ����ͼ��֪pH������2.5ʱȥ�������
�ڸ���ȥ����ͼ��֪pHС��2ʱ��ȥ����Ϊ0��
��� �⣺��1������ʵ����Ʊ���֪��ʵ����̽��Ͷ�ϱȲ�ͬ������������ͬ������ʵ����Ŀ����̽��Ͷ�ϱȶԸý��ⷴӦ���ʵ�Ӱ�죻�����������䣬�ı��¶ȣ���Ӧ���ʸı䣬�����ʵ����ȣ��¶Ȳ�ͬ���ɣ�
�ʴ�Ϊ��̽��Ͷ�ϱȶԸý��ⷴӦ���ʵ�Ӱ�죻4��10��1��318��0��
��2��Ҫ̽����Һ��pH��Fe3+�Ĵ��ڶԸý��ⷴӦ���ʵ�Ӱ�죬������ʵ�������иı�pH��ʵ�顢��Fe3+��ʵ�飬����ʵ����⣬���ٻ������2�Σ�
�ʴ�Ϊ��2��
��3������ȥ����ͼ��֪pH������2.5ʱȥ����������Թ�ҵ��ʹ�ø�����س�ȥ��ˮ�еı���ʱ��pH������2.5��
�ʴ�Ϊ��2.5��
�ڸ���ȥ����ͼ��֪pHС��2ʱ��ȥ����Ϊ0��������ӦҺ�м������ᣬʹ��ҺpH��2����ʹ��Ӧֹͣ��
�ʴ�Ϊ����ӦҺ�м������ᣬʹ��ҺpH��2��
���� ���⿼����̽��Ӱ�컯ѧ��Ӧ���ʵ������Լ���ͼ��������ע�����Ա�ʵ��ʱֻ�ܸı�һ����������������������ͬ���������ó���ȷ���ۣ�


| A�� | ʵ�鷨 | B�� | �۲취 | C�� | �ȽϷ� | D�� | ���෨ |
 ����ˮ�Ǻϳ�ϩ���ij��÷�����ʵ���Һϳɻ���ϩ�ķ�Ӧ���£�
����ˮ�Ǻϳ�ϩ���ij��÷�����ʵ���Һϳɻ���ϩ�ķ�Ӧ���£� $��_{��}^{ŨH_{2}SO_{4}}$
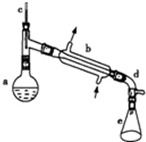
$��_{��}^{ŨH_{2}SO_{4}}$ ��ʵ��װ����ͼ��ʾ�������õ����й����������
��ʵ��װ����ͼ��ʾ�������õ����й����������| ��Է������� | �ܶ�/��g•cm-3�� | �е�/�� | �ܽ��� | |
| ���Ҵ� | 100 | 0.9618 | 161 | ����ˮ |
| ����ϩ | 82 | 0.8102 | 83 | ������ˮ |
��a�м���20g��������2СƬ���Ƭ����ȴ��������������1mLŨ���ᣮb��ͨ����ȴˮ��ʼ��������a�������������¶Ȳ�����90�森
�����ᴿ��������ﵹ���Һ©��������������5%̼������Һ������ˮϴ�ӣ�����������ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ƣ�����ͨ������õ���������ϩ10g��
�ش��������⣺
��1��װ��b�������������ܣ�
��2���������Ƭ�������Ƿ����У��������һ��ʱ��������Ǽ����Ƭ��Ӧ�ò�ȡ����ȷ������B������ȷ�𰸱�ţ�
A���������� B����ȴ�� C�����貹�� D����������
��3����ʵ���������ײ������л�������Ϊ
 ��
����4���ڱ�ʵ���������У�����Ӧ�ôӷ�Һ©�����Ͽڵ�������Ͽڵ��������¿ڷų�������
��5�������ᴿ�����м�����ˮ�Ȼ��Ƶ�Ŀ�������ղ�����������ˮ��
��6����ʵ�����õ��Ļ���ϩ������61%��
| A�� | ��ѧ�뽡�������ˮ�������ڲ���ά���أ��ù�ҵ�Σ��������ƣ������߲� | |
| B�� | ��ѧ����Դ��ú��ʯ�͡���Ȼ�������ڻ�ʯ��Դ�����ܡ�̫���ܵ���������Դ | |
| C�� | ��ѧ��Ӧ�ã���ʳ�׳�ȥˮ���е�ˮ�����û���̿��ȥ�����е���ζ | |
| D�� | ��ѧ�밲ȫ����ȼ��ȼ������ǰ���鴿�������δ�����IJ˽��������ƻ����顱 |
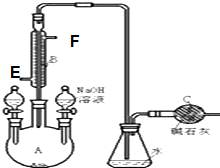 �Ʊ��屽��ʵ��װ����ͼ��ʾ���ش��������⣺
�Ʊ��屽��ʵ��װ����ͼ��ʾ���ش��������⣺
 ʵ���ҳ��ñ���ȩ��Ũ����������Һ���Ʊ����״��ͱ����ᣮ
ʵ���ҳ��ñ���ȩ��Ũ����������Һ���Ʊ����״��ͱ����ᣮ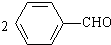 +NaOH��
+NaOH��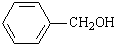 +
+
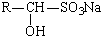 ���������ѣ�������ˮ��
���������ѣ�������ˮ��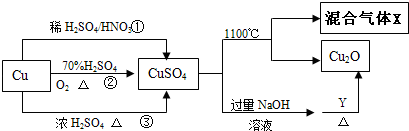
 ��ϵͳ������������3��4-����-3-�һ�����
��ϵͳ������������3��4-����-3-�һ�����