题目内容
5.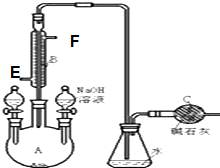 制备溴苯的实验装置如图所示,回答下列问题:
制备溴苯的实验装置如图所示,回答下列问题:(1)仪器A的名称为三颈烧瓶,冷凝管B有E、F两个管口,冷却水应从E处进入.
(2)写出A中苯发生反应的化学方程式

(3)下列说法不正确的是A(单选)
A.三颈烧瓶中左边的分液漏斗中加入的是苯和溴水
B.导管不能插入锥形瓶中的液面之下,目的是防止倒吸
C.锥形瓶中的导管口出现大量白雾
D.碱石灰作用是防止有毒气体逸出,污染环境
(4)右侧分液漏斗中的NaOH溶液在反应反应后时加入A中(填写“反应前”、“反应中”或者“反应后”),用其作用是除去溴苯中的溴,此时液体出现分层现象,下层液体为溴苯(填名称).
分析 本题是依据苯的性质,用苯和溴为原料制备溴苯,并对反应后的混合物进行分离与提纯,得到纯净的溴苯,实验过程中为了防止溴的挥发,需要要安装冷凝装置,冷却水通常是低进高出,反应后的混合物通常用氢氧化钠溶液洗涤后再进行分液,因溴苯的密度比水大,分层后应在下层;
(1)反应容器A是三颈烧瓶,冷却水应从下口流入,上口流出,流速较慢,可达到更好的冷凝效果;
(2)苯和液溴在铁粉作催化剂的作用下生成溴苯和溴化氢,发生取代反应;
(3)反应是利用苯和液溴发生取代反应制备溴苯,结合相关理论去判断;
(4)制备溴苯完成后,加入氢氧化钠溶液除掉过量的Br2和生成的溴化氢,混合液静置分层后,密度大的在下层.
解答 解:(1)仪器A是三颈烧瓶,冷却水应从下口流入,上口流出,流速较慢,可达到更好的冷凝效果,故答案为:三颈烧瓶;E;
(2)苯和液溴取代反应的化学方程式为 ,故答案为:
,故答案为: ;
;
(3)A.三颈烧瓶中左边的分液漏斗中加入的是苯和液溴,错误;
B.为防止倒吸,导管不能插入锥形瓶中的液面之下,正确;
C.反应生成的HBr极易溶解于水,容易在液面上方形成大量白雾,正确;
D.利用碱石灰吸收尾气,防止有毒气体逸出,污染环境,正确;
故答案为:A;
(4)Br2是制备溴苯的反应物,制备溴苯完成后,加入氢氧化钠溶液除掉过量的Br2和生成的溴化氢,混合液静置后,因溴苯的密度比水大,分层后在下层,故答案为:反应后;除去未反应的溴和烧瓶中的HBr;溴苯.
点评 本题考查了溴苯的制备及混合物的分离与提纯,注重了基础知识考查,根据所学知识完成即可,本题难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列关于乙烯的说法不正确的是( )
| A. | 无色气体,难溶于水 | B. | 含有碳碳双键 | ||
| C. | 可使溴水褪色 | D. | 燃烧时产生淡蓝色火焰 |
17.在5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,被氧化的氯元素与被还原的氯元素的质量比为( )
| A. | 1:1 | B. | 5:1 | C. | 1:5 | D. | 3:1 |
14.有一块重36g的薄铁片.将它浸入160g CuSO4溶液中,一段时间后取出铁片洗净后称量,其质量为39.2g.则溶液中Fe2+的物质的量为( )
| A. | 0.45mol | B. | 0.35mol | C. | 0.4mol | D. | 无法计算 |
1.有关金属钠的叙述正确的是 ( )
| A. | 钠的密度比煤油大,保存在煤油中 | |
| B. | 金属钠质软,可以用小刀切割 | |
| C. | 钠的熔点比水大,钠投入到水中放热反应生成的气体中有大量水蒸气 | |
| D. | Na比Cu活泼,因而可以从Cu的盐溶液中置换出铜 |
10. 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
实验步骤如下:
将Na2Cr2O7溶液与浓硫酸混合液放置在B中.在A中加入正丁醇和几粒沸石,加热,保持反应温度为90~95℃,在E中收集90℃以上的馏分.
将馏出物倒入分液漏斗中,除去水层,有机层干燥后蒸馏,收集75~77℃馏分.
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,容易发生迸溅.
(2)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(3)温度计的作用分别是C1C1控制反应温度;C2C2测定蒸馏出来气体的温度.
(4)将正丁醛粗产品置于分液漏斗中水在下层(填“上”或“下”).
(5)反应温度应保持在90~95℃,其原因是既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/℃ | 密度/g•cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
将Na2Cr2O7溶液与浓硫酸混合液放置在B中.在A中加入正丁醇和几粒沸石,加热,保持反应温度为90~95℃,在E中收集90℃以上的馏分.
将馏出物倒入分液漏斗中,除去水层,有机层干燥后蒸馏,收集75~77℃馏分.
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,容易发生迸溅.
(2)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(3)温度计的作用分别是C1C1控制反应温度;C2C2测定蒸馏出来气体的温度.
(4)将正丁醛粗产品置于分液漏斗中水在下层(填“上”或“下”).
(5)反应温度应保持在90~95℃,其原因是既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
14. 高铁酸钾是一种新型非氯高效消毒剂,常用于工业废水与城市生活污水的处理.某小组同学为研究高铁酸钾对水溶液中苯酚的降解反应速率,在恒定实验温度298K或318K条件下(其余实验条件见下表),设计如下对比实验.
高铁酸钾是一种新型非氯高效消毒剂,常用于工业废水与城市生活污水的处理.某小组同学为研究高铁酸钾对水溶液中苯酚的降解反应速率,在恒定实验温度298K或318K条件下(其余实验条件见下表),设计如下对比实验.
(1)请完成下列实验设计表:
(2)若还要探究溶液的pH和Fe3+的存在对该降解反应速率的影响,除实验Ⅰ、Ⅱ、Ⅲ外,至少还需进行2次对比实验.
(3)某同学以实验Ⅰ为参照实验,经过大量实验通过HPLC法测得不同pH下高铁酸钾对水溶液中苯酚的去除率,其结果如图所示.
①工业上使用高铁酸钾除去废水中的苯酚时,pH控制在2.5左右.
②依据图中信息,给出一种使反应停止的方法:向反应液中加入硫酸,使溶液pH<2.
 高铁酸钾是一种新型非氯高效消毒剂,常用于工业废水与城市生活污水的处理.某小组同学为研究高铁酸钾对水溶液中苯酚的降解反应速率,在恒定实验温度298K或318K条件下(其余实验条件见下表),设计如下对比实验.
高铁酸钾是一种新型非氯高效消毒剂,常用于工业废水与城市生活污水的处理.某小组同学为研究高铁酸钾对水溶液中苯酚的降解反应速率,在恒定实验温度298K或318K条件下(其余实验条件见下表),设计如下对比实验.(1)请完成下列实验设计表:
| 实验编号 | pH | 投料比(高铁酸钾与苯酚的质量比) | T/K | Fe3+ | 实验目的 |
| Ⅰ | 4 | 10:1 | 298 | 0 | 参照实验 |
| Ⅱ | 4 | 8:1 | 298 | 0 | |
| Ⅲ | 探究温度对该降解反应速率的影响 |
(3)某同学以实验Ⅰ为参照实验,经过大量实验通过HPLC法测得不同pH下高铁酸钾对水溶液中苯酚的去除率,其结果如图所示.
①工业上使用高铁酸钾除去废水中的苯酚时,pH控制在2.5左右.
②依据图中信息,给出一种使反应停止的方法:向反应液中加入硫酸,使溶液pH<2.
15.下列离子方程式书写正确的是( )
| A. | 碳酸钠溶液中逐滴加入与之等物质的量的盐酸:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O | |
| B. | 向碳酸氢钡溶液中加入少许氢氧化钠:Ba2++HCO${\;}_{3}^{-}$+OH-═BaCO3↓+H2O | |
| C. | 向次氯酸钙溶液中通入过量的二氧化硫气体:SO2+H2O+ClO-═HSO${\;}_{3}^{-}$+HClO | |
| D. | 向复盐(NH4)2Fe(SO4)2溶液中加少许Ba(OH)2:SO${\;}_{4}^{2-}$+2NH${\;}_{4}^{+}$+Ba2++2OH-═BaSO4↓+2NH3+H2O |