题目内容
12.已知某有机物的结构简式如图所示:下列有关说法正确的是( )
| A. | 该有机物的化学式为C11H12OCl2 | |
| B. | 在同一平面上的碳原子数最多为10个 | |
| C. | 与NaOH醇溶液在加热条件下消去氯原子 | |
| D. | 在铜作催化剂和加热条件下能被O2氧化成醛 |
分析 该物质中含有苯环、醇羟基、碳碳双键、氯原子,所以具有苯、醇、烯烃、卤代烃的性质,能发生加成反应、氧化反应、取代反应、消去反应、加聚反应等,据此分析解答.
解答 解:A.根据结构简式知其分子式为C11H12OCl2,故A正确;
B.直接连接苯环的碳原子、连接碳碳双键的碳原子能共面,甲基上C原子和连接甲基的碳原子可能共平面,所以在同一平面上的碳原子数最多为11个,故B错误;
C.苯环上的氯原子不能发生消去反应,苯环上甲基上的氯原子不能发生消去反应,故C错误;
D.醇羟基没有位于边上,所以发生催化氧化反应时生成酮而不是醛,故D错误;
故选A.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系是解本题关键,难点是原子共面判断,以苯、乙烯为模型采用知识迁移方法解答,题目难度不大.

练习册系列答案
相关题目
20.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.请回答下列问题:
(1)上述实验中发生反应的化学方程式有Zn+CuSO4=ZnSO4+Cu、Zn+H2SO4=ZnSO4+H2↑;
(2)硫酸铜溶液可以加快氢气生成速率的原因是通过一系列反应构成了Cu/Zn原电池,该原电池的电极反应式,负极:Zn-2e-=Zn2+;正极:2H++2e-=H2↑
(3)要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度、适当增加硫酸的浓度、增加锌粒的表面积等(答两种).
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
①请完成此实验设计,其中:V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入的CuSO4溶液超过一定量时,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积.
(1)上述实验中发生反应的化学方程式有Zn+CuSO4=ZnSO4+Cu、Zn+H2SO4=ZnSO4+H2↑;
(2)硫酸铜溶液可以加快氢气生成速率的原因是通过一系列反应构成了Cu/Zn原电池,该原电池的电极反应式,负极:Zn-2e-=Zn2+;正极:2H++2e-=H2↑
(3)要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度、适当增加硫酸的浓度、增加锌粒的表面积等(答两种).
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL-1 | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL-1 | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL-1 | V7 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入的CuSO4溶液超过一定量时,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积.
7.下列关于有机物的说法中,错误的是( )
| A. | 在一定条件下葡萄糖能与新制Cu(OH)2发生反应 | |
| B. | 肥皂的主要成分是油脂在碱性条件下水解生成的 | |
| C. | 淀粉、纤维素和油脂都是天然高分子化合物 | |
| D. | 蛋白质溶液遇硫酸铜后产生的沉淀不能重新溶于水 |
17.下列推断合理的是( )
| A. | 明矾[KAl(SO4)2•12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 | |
| B. | 向50mL 18mol/L 硫酸中加入足量铜片并加热,被还原硫酸的物质的量是0.45mol | |
| C. | 浓硫酸溅到皮肤上,立即用碳酸钠稀溶液冲洗 | |
| D. | 将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水色后加热也能恢复原色 |
4.下列事实可以表明醋酸是弱电解质的是( )
| A. | 醋酸能与水任意比例互溶 | |
| B. | 醋酸溶液的导电能力比盐酸弱 | |
| C. | 醋酸溶液中存在醋酸根离子、氢离子 | |
| D. | 常温下,1 mol•L-1的醋酸中c(H+)约为0.01 mol•L-1 |
1.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 1molCH4分子中共价键总数为4NA | |
| B. | 18gD2O中含有的质子数目为10NA | |
| C. | 标准状况下,5.6LCCl4含有的分子数为0.25NA | |
| D. | 28gN2和1molCH2=CH2所含电子数都是14NA |
2.下列有关化学用语使用正确的是( )
| A. | 乙醇分子比例模型: | |
| B. | 醛基的电子式: | |
| C. |  的名称为:2,4,4-三甲基-1-戊烯 的名称为:2,4,4-三甲基-1-戊烯 | |
| D. | 乙酸、葡萄糖、淀粉的最简式均为CH2O |

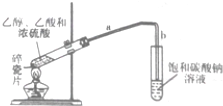 合成乙酸乙酯的路线如下:
合成乙酸乙酯的路线如下: .
.