题目内容
11.下列表达式正确的是( )| A. | NaHCO3的电离:NaHCO3═H++CO32-+Na+ | |
| B. | Na2S的水解:S2-+2H2O?H2S+2OH- | |
| C. | CH3COONH4的电离:CH3COONH4═NH4++CH3COO- | |
| D. | FeCl3的水解:Fe3++3H2O?Fe(OH)3↓+3H+ |
分析 A.碳酸氢根离子为弱酸的酸式根离子,不能拆;
B.硫离子为多元弱酸根离子,分步水解,以第一步为主;
C.醋酸铵为强电解质,完全电离;
D.盐类水解为微弱的,电离生成氢氧化铁少量不能标注沉淀,应用可逆符号.
解答 解:A.NaHCO3是强电解质,完全电离:NaHCO3═HCO3-+Na+,故A错误;
B.Na2S的水解,离子方程式:S2-+H2O?HS-+OH-,故B错误;
C.CH3COONH4的电离,离子方程式:CH3COONH4═NH4++CH3COO-,故C正确;
D.FeCl3的水解离子方程式:Fe3++3H2O?$\stackrel{.}{?}$Fe(OH)3+3H+,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意电解质强弱及电离方式,题目难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
1.将铁片和铜片用导线连接置于同一浓硝酸溶液中,下列各叙述正确的是( )
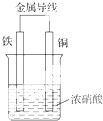

| A. | 铁片上发生氧化反应Fe-3e-═Fe3+ | B. | 铜片上发生还原反应2H++2e-═H2↑ | ||
| C. | 铜片上发生氧化反应Cu-2e-═Cu2+ | D. | 溶液中NO${\;}_{3}^{-}$的浓度基本不变 |
19.下列叙述正确的是( )
| A. | 日常生活中用无水乙醇杀菌消毒 | |
| B. | 目前加碘食盐中添加的是KIO3 | |
| C. | 绿色食品是不含任何化学物质的食品 | |
| D. | 碘是人体中含量最多的必需微量元素 |
6.能用H++OH-═H2O表示的是( )
| A. | Ba(OH)2溶液和稀H2SO4的反应 | B. | Cu(OH)2和稀H2SO4的反应 | ||
| C. | NaOH溶液和氢溴酸反应 | D. | NaOH溶液和醋酸溶液的反应 |
16.下列物质属于电解质的是( )
| A. | 碘酒 | B. | 液氯 | C. | HClO | D. | 氯水 |
3.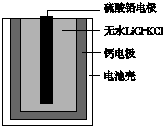 热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )
热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )
 热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )
热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )| A. | 常温时,在正负极间接上电流表或检流计,指针不偏转 | |
| B. | 放电过程中,Li+向负极移动 | |
| C. | 每转移0.2mol电子,理论上生成41.4gPb | |
| D. | 正极反应式:Ca+2Cl--2e-═CaCl2 |
1.如图装置或实验操作不正确的是( )
| A. | 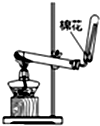 实验室制取并收集NH3 实验室制取并收集NH3 | B. | 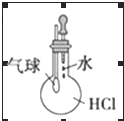 验证HCl气体的溶解性 验证HCl气体的溶解性 | ||
| C. | 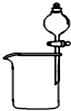 分离碘酒中的碘和酒精 分离碘酒中的碘和酒精 | D. | 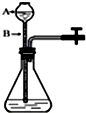 检查装置的气密性 检查装置的气密性 |
 .
.