题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1 NaHSO4溶液:K+、Fe2+、NO3-、Cl-
B.0.1 mol·L-1NaAlO2的溶液:K+、Na+、SO42-、CO32-
C.无色溶液:Ba 2+、Na+、MnO4-、NO3-
D.由水电离出的c(OH-)=1.0×10-12 mol·L-1的溶液:NH4+、HCO3-、Na+、Cl-
B
【解析】
试题分析:A.0.1 mol·L-1 NaHSO4溶液是强酸性溶液,会发生反应:3Fe2++NO3-+4H+= 3Fe3++NO↑+2H2O。不能大量共存。错误。B.0.1 mol·L-1NaAlO2的溶液,离子K+、Na+、SO42-、CO32-不会发生任何反应,可以大量共存。正确。C.MnO4-是紫色的,在无色溶液中不能大量存在。错误。D.常温下纯水电离出的c(OH-)=1.0×10-7mol/L.现在由水电离出的c(OH-)=1.0×10-12 mol·L-1的溶液,说明该溶液可能是酸性溶液,也可能是碱性溶液。在酸性溶液中会发生反应:HCO3-+H+=CO2↑+H2O;在碱性溶液中会发生反应:HCO3-+OH-=CO32-+H2O;NH4++OH-=NH3·H2O,因此不能大量共存。错误。
考点:考查离子能否大量共存的知识。

(14分)二甲醚(CH3OCH3)和甲醇(CH3OH)都是高效清洁能源。工业上利用煤的气化产物(水煤气)合成甲醇和二甲醚。回答下列问题:
(1)制备二甲醚最后一步反应由Al2O3催化甲醇脱水合成,反应方程式为 。
(2)已知:CO(g)+2H2(g)=CH3OH (g) △H= —90.1kJ·mol-1 CO(g)的燃烧热是282.8 kJ·mol-1;H2的燃烧热是285.8 kJ·mol-1写出表示CH3OH (g) 燃烧热的热化学反应方程式 。
(3)二甲醚直接燃料电池比甲醇直接燃料电池更高效,等质量的二甲醚和甲醇完全放电转移电子的物质的量之比是 。用二甲醚直接燃料电池电解足量饱和食盐水,当消耗9.2g二甲醚时理论上阴极产生的气体的体积为 L。(标况下)
(4)在合成中伴有水煤气交换反应:CO(g)+H2O(g)  CO2(g)+H2(g),等物质的量的CO(g)和H2O(g)加入密闭容器中反应,平衡时测得结果如下表。
CO2(g)+H2(g),等物质的量的CO(g)和H2O(g)加入密闭容器中反应,平衡时测得结果如下表。
温度 | 260℃ | 280℃ | 295℃ | 310℃ |
CO转化率 | 89% | 80% | 75% | 60% |
①请解释CO转化率随温度变化的关系 。
②列式计算280℃时平衡常数 。
③若平衡体系中,测得H2的压强占总压的30%,要使体系中CO转化率达到70%,应该使温度 (填“升高”、“降低”、“不变”)
(本题共15分)
有4种质量比可能相同或不同的镁铝合金样品①、②、③、④。甲、乙、丙、丁4位同学各取1种样品,进行下列实验,测定合金中镁的质量分数。
52.甲同学取样品①m1 g和过量的氢氧化钠溶液反应,然后过滤;再往滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m1 g。则样品①合金中镁的质量分数为_____________。
53.乙同学取样品②m2 g和足量的盐酸反应,然后滴加过量的氢氧化钠溶液,将沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m2 g。则样品②合金中镁的质量分数为____________。
54.丙同学取样品③m3 g和足量的稀硫酸反应,发现固体完全溶解,标准状况下得到气体体积为V L,则样品③中m3的取值范围是___________________________________________。
丁同学取不同质量的样品④分别和30 mL同浓度的盐酸反应,所取合金质量与产生气体体积(已转化为标准状况)如下:
实验序号 | a | b | c |
合金质量/mg | 510 | 765 | 918 |
气体体积/mL | 560 | 672 | 672 |
55.通过计算求该盐酸的物质的量浓度。
56.通过计算求样品④中合金中镁的质量分数。
57.在c组实验后,还需向容器中加入1.0 mol·L-1的氢氧化钠溶液多少毫升才能使剩余合金中的铝恰好完全溶解?
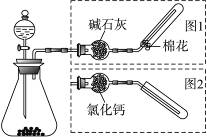
下图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示。下列选项中正确的是
选项 | 发生装置中的药品 | 干燥和集气装置 |
A | 电石和饱和食盐水 | 图2 |
B | 大理石和稀盐酸 | 图1 |
C | 铜和稀硝酸 | 图2 |
D | 氧化钙和浓氨水 | 图1 |