题目内容
2.主族元素R的最高正化合价为+5,R元素位于周期表的( )| A. | ⅠA族 | B. | ⅡA族 | C. | ⅢA族 | D. | ⅤA族 |
分析 主族元素的最高正价=元素原子的最外层电子数=主族序数,据此回答.
解答 解:主族元素R的最高正化合价为+5,则主族元素的最高正价=元素原子的最外层电子数=主族序数=5,所以是第ⅤA族元素.
故选D.
点评 本题考查元素周期律的有关知识,注意主族元素的最高正价=元素原子的最外层电子数=主族序数这一规律的把握,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.在下列五种物质的组合中,既能跟氢氧化钠溶液反应,又能跟盐酸反应的化合物是( )
①Al ②Al(OH)3 ③Al2O3 ④Na2CO3 ⑤NaHCO3.
①Al ②Al(OH)3 ③Al2O3 ④Na2CO3 ⑤NaHCO3.
| A. | ①②③ | B. | ①③⑤ | C. | ②③⑤ | D. | ②④⑤ |
10.下列鉴别方法可行的是( )
| A. | 用氨水鉴别MgCl2溶液和AlCl3溶液 | |
| B. | 用二氧化碳鉴别CaCl2溶液和NaCl溶液 | |
| C. | 用铁片鉴别稀H2SO4和浓H2SO4 | |
| D. | 用相互滴加的方法鉴别NaHCO3溶液和Ca(OH)2溶液 |
17.下列所用除杂的试剂和操作方法均正确的是( )
| 选项 | 物质 | 杂质 | 所用试剂 | 操作方法 |
| ① | 乙烯 | 二氧化硫 | KMnO4溶液 | 洗气 |
| ② | 乙炔 | 硫化氢 | 氢氧化钠溶液 | 洗气 |
| ③ | 苯 | 甲苯 | 溴水 | 分液 |
| ④ | 溴苯 | 液溴 | 氢氧化钠溶液 | 分液 |
| A. | ②③ | B. | ①④ | C. | ②④ | D. | ①③ |
7.下列说法中,正确的是( )
| A. | s区元素都是金属元素 | B. | p区元素全部都是非金属元素 | ||
| C. | d区、ds区和f区由副族元素组成 | D. | s区和p区由主族和0族元素组成 |
14.下列说法中正确的是( )
| A. | 原子晶体中的各相邻原子都以共价键相结合 | |
| B. | 金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | |
| C. | 分子晶体的熔沸点很低,常温下都呈液态或气态 | |
| D. | 离子晶体中每个离子周围均吸引着6个带相反电荷的离子 |
11.已知烯烃在一定条件下氧化时, 键断裂.如RCH═CHR′可氧化成RCHO和R′CHO,下列烯烃中,经氧化可得到乙醛和丁醛的是( )
键断裂.如RCH═CHR′可氧化成RCHO和R′CHO,下列烯烃中,经氧化可得到乙醛和丁醛的是( )
 键断裂.如RCH═CHR′可氧化成RCHO和R′CHO,下列烯烃中,经氧化可得到乙醛和丁醛的是( )
键断裂.如RCH═CHR′可氧化成RCHO和R′CHO,下列烯烃中,经氧化可得到乙醛和丁醛的是( )| A. | 1-己烯 | B. | 2-己烯 | C. | 3-已烯 | D. | 2-甲基-2-戊烯 |
12.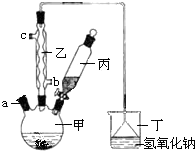 溴苯是一种化工原料,实验室用以下甲、乙、丙、丁等仪器组合,合成溴苯的装置示意图(其余辅助仪器略去)及有关数据如下,按要求回答下列问题:
溴苯是一种化工原料,实验室用以下甲、乙、丙、丁等仪器组合,合成溴苯的装置示意图(其余辅助仪器略去)及有关数据如下,按要求回答下列问题:
(1)仪器乙的名称为:球型冷凝管;
(2)用如图的装置制备溴苯时的操作为:向甲中预先加入少量铁屑,再加入适量苯,丙中预先装好适量液溴,将丙中所装的液溴缓慢滴入甲中,充分反应.反应中铁屑的作用是:催化剂;
写出制备溴苯的化学反应方程式是:C6H6+Br2$\stackrel{Fe}{→}$C6H5Br+HBr;
(3)丁装置烧杯中倒置的漏斗的目的是:防倒吸;
写出丁中发生的主要化学反应的方程式为:NaOH+HBr=NaBr+H2O;
(4)充分反应后,向甲中加入适量水,然后过滤除去未反应的铁屑;所得到滤液就是制得的粗溴苯,其中含有未反应完的液溴,最好应选择试剂A除去,
A 氢氧化钠溶液 B稀盐酸溶液 C氯化钠溶液 D水
经过上述操作所得的粗溴苯中还含有杂质苯,要进一步提纯,应选下列哪种操作G除去.
E 重结晶 F 过滤 G 蒸馏 H 萃取.
 溴苯是一种化工原料,实验室用以下甲、乙、丙、丁等仪器组合,合成溴苯的装置示意图(其余辅助仪器略去)及有关数据如下,按要求回答下列问题:
溴苯是一种化工原料,实验室用以下甲、乙、丙、丁等仪器组合,合成溴苯的装置示意图(其余辅助仪器略去)及有关数据如下,按要求回答下列问题:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/°C | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
(2)用如图的装置制备溴苯时的操作为:向甲中预先加入少量铁屑,再加入适量苯,丙中预先装好适量液溴,将丙中所装的液溴缓慢滴入甲中,充分反应.反应中铁屑的作用是:催化剂;
写出制备溴苯的化学反应方程式是:C6H6+Br2$\stackrel{Fe}{→}$C6H5Br+HBr;
(3)丁装置烧杯中倒置的漏斗的目的是:防倒吸;
写出丁中发生的主要化学反应的方程式为:NaOH+HBr=NaBr+H2O;
(4)充分反应后,向甲中加入适量水,然后过滤除去未反应的铁屑;所得到滤液就是制得的粗溴苯,其中含有未反应完的液溴,最好应选择试剂A除去,
A 氢氧化钠溶液 B稀盐酸溶液 C氯化钠溶液 D水
经过上述操作所得的粗溴苯中还含有杂质苯,要进一步提纯,应选下列哪种操作G除去.
E 重结晶 F 过滤 G 蒸馏 H 萃取.
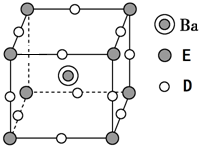 有原子序数依次增大的A、B、C、D、E、F、G 七种元素,A 是短周期中族序数等于周期数的非金属元素;B 元素的原子既不易失去也不易得到电子,其基态原子中每种能级电子数相同;D 的最外层电子数与电子层数之比为3:1;E是地壳中含量第二多的非金属元素;D、F同族; G 元素原子序数为24.
有原子序数依次增大的A、B、C、D、E、F、G 七种元素,A 是短周期中族序数等于周期数的非金属元素;B 元素的原子既不易失去也不易得到电子,其基态原子中每种能级电子数相同;D 的最外层电子数与电子层数之比为3:1;E是地壳中含量第二多的非金属元素;D、F同族; G 元素原子序数为24.