题目内容
14.下列说法中正确的是( )| A. | 原子晶体中的各相邻原子都以共价键相结合 | |
| B. | 金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | |
| C. | 分子晶体的熔沸点很低,常温下都呈液态或气态 | |
| D. | 离子晶体中每个离子周围均吸引着6个带相反电荷的离子 |
分析 A、原子晶体中原子间作用力为共价键;
B、金属导电的原因是有自由电子,金属里本来就存在有自由电子;
C、分子晶体存在常温下呈固态的物质;
D、离子所带电荷数和离子半径的大小不同,每个离子周围均吸引带相反电荷的离子数目不同.
解答 解:A、原子晶体中原子间作用力为共价键,故A正确;
B、金属里本来就存在有自由电子,在金属未通电的情况下,金属中的电子是在做热运动,即无规则运动,在外加电场的作用下自由电子做定向移动,而不是产生了自由电子,故B错误;
C、分子晶体存在常温下呈固态的物质,例如S、白磷、红磷、C60等都属于分子晶体,在常温下为固态,故C错误;
D、离子所带电荷数和离子半径的大小不同,每个离子周围均吸引带相反电荷的离子数目不同,一个NaCl晶胞为立方体,Na+离子在立方体中心的话,离它最近的Cl-离子在立方体六个面的中央,CsCl的晶胞也是立方体,Cs+离子在立方体中心的话,离它最近的Cl-离子就在立方体的八个顶点上,故D错误.
故选A.
点评 本题考查晶体的类型与性质,题目难度不大,注意晶体的组成、结构、性质等知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列元素中,最高正化合价数值最大的是( )
| A. | Cl | B. | O | C. | Mg | D. | Na |
5.有关晶体的下列说法中正确的是( )
| A. | 原子晶体中共价键越强,熔点越高 | |
| B. | 晶体中分子间作用力越大,分子越稳定 | |
| C. | 冰融化时水分子中共价键发生断裂 | |
| D. | 氯化钠熔化时离子键未被破坏 |
2.主族元素R的最高正化合价为+5,R元素位于周期表的( )
| A. | ⅠA族 | B. | ⅡA族 | C. | ⅢA族 | D. | ⅤA族 |
9.下表是元素周期表的一部分,用化学符号回答下列有关问题:
(1)写出下列元素的符号:①N,⑥Si,⑦S.
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,称为两性氢氧化物的是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.
(5)在③与④,化学性质较活泼的是Na.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | (11) | (12) |
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,称为两性氢氧化物的是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.
(5)在③与④,化学性质较活泼的是Na.
19.短周期元素X和Y,X原子的电子层数为n,最外层电子数为(2n+1),Y原子最外层电子数是次外层电子数的3倍.下列说法一定正确的是( )
| A. | X和Y都是非金属元素,其中X的最高化合价为+5价 | |
| B. | X与Y所能形成的化合物都是酸性氧化物 | |
| C. | 元素X的氧化物的水化物是强酸 | |
| D. | X的氢化物极易溶于水,可以用来做喷泉实验 |
6.常温常压下,将盛有20mL NO2和O2的混合气体的大试管倒立在水槽中,水面上升至一定位置后不再变化,此时还有3mL气体,则原混合气体中的NO2的体积可能是( )
| A. | 17.8 mL | B. | 14.8 mL | C. | 12.6 mL | D. | 12.4 mL |
 上世纪60年代,第一个稀有气体化合物Xe[PtF6]被合成出来后,打破了“绝对惰性”的观念.在随后的几年内,科学家又相继合成了氙的氟化物、氧化物等.
上世纪60年代,第一个稀有气体化合物Xe[PtF6]被合成出来后,打破了“绝对惰性”的观念.在随后的几年内,科学家又相继合成了氙的氟化物、氧化物等.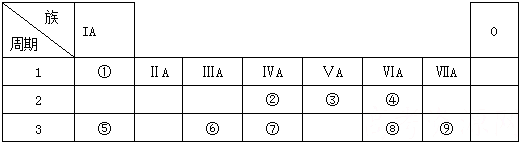
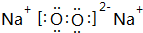 ,含有的化学键类型有离子键、共价键
,含有的化学键类型有离子键、共价键