题目内容
【题目】下列各表述与示意图一致的是( )
A.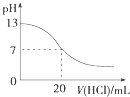
图表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的pH随加入酸体积的变化
B.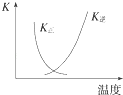 图中曲线表示反应2SO2(g)+O2(g)2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化
图中曲线表示反应2SO2(g)+O2(g)2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化
C.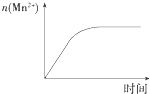
图表示10 mL 0.01 molL﹣1 KMnO4酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+)随时间的变化
D.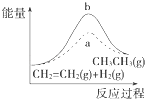
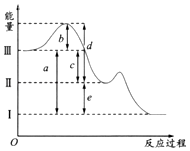
图中a、b曲线分别表示反应CH2═CH2(g)+H2(g)﹣→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化
【答案】B
【解析】解:A.用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1NaOH溶液的pH随加入盐酸体积的变化,pH会突变,故A错误;
B.2SO2(g)+O2(g)2SO3(g)△H<0,升高温度平衡向吸热方向移动,即向逆方向移动,则逆方向是平衡常数增大,正方向的平衡常数减小,图象符合,故B正确;
C.反应中生成的Mn2+对该反应有催化作用,反应过程中溶液中锰离子浓度逐渐增大,所以反应速率先慢后快,图象不符合,故C错误;
D.CH2═CH2(g)+H2(g)﹣→CH3CH3(g)△H<0,属于放热反应,放热反应中反应物的总能量大于生成物的总能量,图象不符合,故D错误.
故选B.
【考点精析】通过灵活运用反应热和焓变和化学平衡状态本质及特征,掌握在化学反应中放出或吸收的热量,通常叫反应热;化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)即可以解答此题.

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案