题目内容
 碱式碳酸铜 Cu2(OH)2CO3是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜 Cu2(OH)2CO3是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
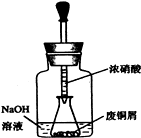
步骤一:废铜屑制硝酸铜:如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液.
步骤二:碱式碳酸铜的制备:向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品.完成下列填空:
①如图装置中NaOH溶液的作用是________.反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有________(填写化学式).
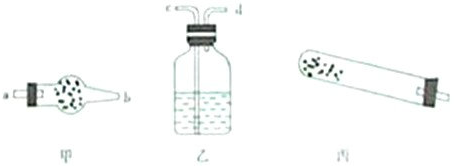
②步骤二中,水浴加热所需仪器有________、________(加热、夹持仪器、石棉网除外);洗涤的目的是________.
③步骤二的滤液中可能含有CO32-,写出检验CO32-的方法.
④若实验得到2.42g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80g固体,此样品中碱式碳酸铜的质量分数是________.
吸收氮氧化物 NaNO2、NaNO3 烧杯 温度计 除去碱式碳酸铜表面的吸附的硝酸钠 92%
分析:广口瓶内铜与浓硝酸反应生成大气污染气体NOx,NaOH溶液可用来吸收NOx,利用NO2+NaOH→NaNO2+NaNO3+H2O可知,反应结束后,广口瓶的溶液中,除了剩余的NaOH外,还含有新生成的NaNO2与NaNO3;因反应器为大试管,故水浴加热中用来盛放水的仪器可以选用烧杯、温度计(测定水温);洗涤可除去碱式碳酸铜表面的吸附的硝酸钠.碱式碳酸铜完全分解得到CuO,设样品中碱式碳酸铜的质量分数为x,依据碱式碳酸铜的方程式,利用“差量法”计算得到所求量,可得:222:62=2.42x:(2.42-1.80),解得x=0.92;
解答:①广口瓶内铜与浓硝酸反应生成大气污染气体NOx,NaOH溶液可用来吸收NOx,利用NO2+NaOH→NaNO2+NaNO3+H2O可知,反应结束后,广口瓶的溶液中,除了剩余的NaOH外,还含有新生成的NaNO2与NaNO3;
故答案为:吸收氮氧化物,NaNO2、NaNO3;
②因反应器为大试管,故水浴加热中用来盛放水的仪器可以选用烧杯、温度计(测定水温);洗涤可除去碱式碳酸铜表面的吸附的硝酸钠;
故答案为:烧杯、温度计;除去碱式碳酸铜表面的吸附的硝酸钠;
③滤液中可能含有CO32-,检验CO32-的方法是:取试样于试管中,加入稀盐酸,将产生的气体通入澄清石灰水中,溶液变浑浊证明含碳酸根离子;
故答案为:取试样于试管中,加入稀盐酸,将产生的气体通入澄清石灰水中,溶液变浑浊证明含碳酸根离子;
④碱式碳酸铜完全分解得到CuO,设样品中碱式碳酸铜的质量分数为x,依据碱式碳酸铜的方程式,Cu2(OH)2CO3=2CuO+CO2↑+H2O;利用“差量法”计算可得:222:62=2.42x:(2.42-1.80),解得x=0.92=92%;
故答案为:0.92或92%;
点评:本题考查了铜及其化合物性质的应用,制备实验方案的设计和分析判断,实验仪器的使用,离子检验方法的应用,化学方程式计算应用.
分析:广口瓶内铜与浓硝酸反应生成大气污染气体NOx,NaOH溶液可用来吸收NOx,利用NO2+NaOH→NaNO2+NaNO3+H2O可知,反应结束后,广口瓶的溶液中,除了剩余的NaOH外,还含有新生成的NaNO2与NaNO3;因反应器为大试管,故水浴加热中用来盛放水的仪器可以选用烧杯、温度计(测定水温);洗涤可除去碱式碳酸铜表面的吸附的硝酸钠.碱式碳酸铜完全分解得到CuO,设样品中碱式碳酸铜的质量分数为x,依据碱式碳酸铜的方程式,利用“差量法”计算得到所求量,可得:222:62=2.42x:(2.42-1.80),解得x=0.92;
解答:①广口瓶内铜与浓硝酸反应生成大气污染气体NOx,NaOH溶液可用来吸收NOx,利用NO2+NaOH→NaNO2+NaNO3+H2O可知,反应结束后,广口瓶的溶液中,除了剩余的NaOH外,还含有新生成的NaNO2与NaNO3;
故答案为:吸收氮氧化物,NaNO2、NaNO3;
②因反应器为大试管,故水浴加热中用来盛放水的仪器可以选用烧杯、温度计(测定水温);洗涤可除去碱式碳酸铜表面的吸附的硝酸钠;
故答案为:烧杯、温度计;除去碱式碳酸铜表面的吸附的硝酸钠;
③滤液中可能含有CO32-,检验CO32-的方法是:取试样于试管中,加入稀盐酸,将产生的气体通入澄清石灰水中,溶液变浑浊证明含碳酸根离子;
故答案为:取试样于试管中,加入稀盐酸,将产生的气体通入澄清石灰水中,溶液变浑浊证明含碳酸根离子;
④碱式碳酸铜完全分解得到CuO,设样品中碱式碳酸铜的质量分数为x,依据碱式碳酸铜的方程式,Cu2(OH)2CO3=2CuO+CO2↑+H2O;利用“差量法”计算可得:222:62=2.42x:(2.42-1.80),解得x=0.92=92%;
故答案为:0.92或92%;
点评:本题考查了铜及其化合物性质的应用,制备实验方案的设计和分析判断,实验仪器的使用,离子检验方法的应用,化学方程式计算应用.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
 铁、铜和铝是人类生活中常用的金属.
铁、铜和铝是人类生活中常用的金属.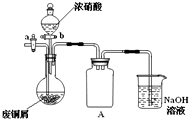 碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下: