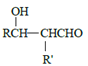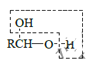题目内容
【题目】水热法制备Fe3O4纳米颗粒的总反应的离子方程式为3Fe2++2![]() +O2+4OH-===Fe3O4+
+O2+4OH-===Fe3O4+![]() +2H2O。下列说法正确的是()
+2H2O。下列说法正确的是()
A.O2和![]() 是氧化剂,Fe2+是还原剂
是氧化剂,Fe2+是还原剂
B.参加反应的氧化剂与还原剂的物质的量之比为1∶5
C.每生成1mol![]() 转移2mol电子
转移2mol电子
D.每2molFe2+被氧化,则被Fe2+还原的O2为0.5mol
【答案】D
【解析】
在3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O中,化合物中铁元素、硫元素用平均化合价,铁元素的化合价变化:+2→![]() ;硫元素的化合价变化为:+2→+2.5;氧元素的化合价变化:0→-2,据此解答。
;硫元素的化合价变化为:+2→+2.5;氧元素的化合价变化:0→-2,据此解答。
A.化合物中铁元素、硫元素用平均化合价,铁元素的化合价变化:+2→![]() ;硫元素的化合价变化为:+2→+2.5;氧元素的化合价变化:0→-2,所以氧化剂是O2;还原剂是Fe2+、S2O32-,故A错误;
;硫元素的化合价变化为:+2→+2.5;氧元素的化合价变化:0→-2,所以氧化剂是O2;还原剂是Fe2+、S2O32-,故A错误;
B.由上述分析可知,氧化剂是O2,还原剂是Fe2+、S2O32-,3molFe2+参加反应时只有2mol被氧化,参加反应的氧化剂与还原剂的物质的最之比为1:(2+2)=1:4,故B错误;
C.由方程式可知,每生成1molFe3O4,参加反应的氧气为1mol,转移电子为1mol×4=4mol,故C错误;
D.2molFe2+被氧化时,失去电子2mol,则被Fe2+还原的O2的物质的量为2mol÷4=0.5mol,故D正确;
答案选D。

练习册系列答案
相关题目
【题目】下列各组物质中,能一步实现下图所示①~⑤转化关系的是

X | Y | Z | W | |
A | C | CO | CO2 | Na2CO3 |
B | Fe3O4 | Fe | FeCl2 | FeCl3 |
C | H2SO4 | SO2 | S | SO3 |
D | Al | Al2O3 | NaAlO2 | Al(OH)3 |
A. A B. B C. C D. D