题目内容
19.下列物质中能跟溴水、酸化高锰酸钾溶液、新制Cu(OH)2溶液、碳酸氢钠溶液都反应的是( )| A. | CH2=CH2 | B. | C6H5OH | C. | 裂化汽油 | D. | 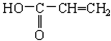 |
分析 能和溴水反应的有机物具有醛基或碳碳不饱和键或酚羟基,能被酸性高锰酸钾溶液氧化的物质含有醛基、碳碳不饱和键或连接苯环碳原子上含有氢原子的苯的同系物,能和新制氢氧化铜悬浊液反应的物质含有醛基或羧基,能和碳酸氢钠反应的物质含有醛基,据此分析解答.
解答 解:能和溴水反应的有机物具有醛基或碳碳不饱和键或酚羟基,能被酸性高锰酸钾溶液氧化的物质含有醛基、碳碳不饱和键或连接苯环碳原子上含有氢原子的苯的同系物,能和新制氢氧化铜悬浊液反应的物质含有醛基或羧基,能和碳酸氢钠反应的物质含有醛基,
A.乙烯中含有碳碳双键,所以能和溴发生加成反应、能和酸性高锰酸钾溶液发生氧化反应,和新制氢氧化铜、碳酸氢钠不反应,故A错误;
B.苯酚中含有酚羟基,能和溴发生取代反应、能被酸性高锰酸钾溶液氧化,和新制氢氧化铜、碳酸氢钠不反应,故B错误;
C.裂化汽油中含有不饱和烃,所以能和溴发生加成反应、能和酸性高锰酸钾溶液发生氧化反应,和新制氢氧化铜、碳酸氢钠不反应,故C错误;
D.该物质中含有碳碳双键和羧基,能和溴发生加成反应、能被酸性高锰酸钾溶液氧化、能和新制氢氧化铜发生中和反应、能和碳酸氢钠反应生成二氧化碳,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,知道常见官能团的性质,注意羧基能和新制氢氧化铜悬浊液发生中和反应,为易错点.

练习册系列答案
相关题目
10.如图是CO2电催化还原为CH4的工作原理示意图.正确的是( )
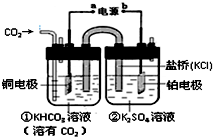

| A. | 该装置为原电池,其中a为正极 | |
| B. | 铜电极的电极反应式为:CO2+8H++8e-$?_{加热}^{催化剂}$CH4+2H2O | |
| C. | 反应开始后,电子从a极流出至铜电极,经电解质溶液到铂电极最后流回至b极 | |
| D. | 一段时间后,②池中溶液的pH一定下降 |
14. 某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.
某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
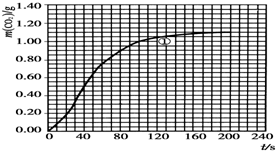
(2)实验①中CO2质量随时间变化的关系见图:
依据反应方程式$\frac{1}{2}$CaCO3+HNO3═$\frac{1}{2}$Ca(NO3)2+$\frac{1}{2}$CO2↑+$\frac{1}{2}$H2O,计算实验①在70~90s范围内HNO3的反应速率(忽略溶液体积变化,写出计算过程).
 某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.
某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol•L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3的浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究大理石规格 (粗、细)对该反应速率 的影响. |
| ② | ||||
| ③ | ||||
| ④ |
依据反应方程式$\frac{1}{2}$CaCO3+HNO3═$\frac{1}{2}$Ca(NO3)2+$\frac{1}{2}$CO2↑+$\frac{1}{2}$H2O,计算实验①在70~90s范围内HNO3的反应速率(忽略溶液体积变化,写出计算过程).
4.下列气体不能用浓硫酸作干燥剂的是( )
①HCl ②NH3 ③Cl2 ④H2 ⑤SO2?⑥HI.
①HCl ②NH3 ③Cl2 ④H2 ⑤SO2?⑥HI.
| A. | ①②⑥ | B. | ②⑤⑥ | C. | ①⑥ | D. | ②⑥ |
8.下列实验能获得成功的是( )
| A. | 在某淀粉溶液中加入适量的稀硫酸,并加热一段时间,待冷却后,再加入银氨溶液来检验淀粉是否已发生水解 | |
| B. | 把R-X与NaOH水溶液混合,加入硝酸银溶液来验证R-X是否为碘代烷 | |
| C. | 在三颈烧瓶中先加入少量铁粉,再加入5mL苯和1mL液溴的混合物,待充分反应后可制得少量溴苯 | |
| D. | 将无水乙醇和浓硫酸共热至140℃可制得乙烯 |
 ,工业合成路线如下:
,工业合成路线如下:

 (R-代表烃基)
(R-代表烃基) 、
、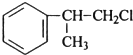 ;
;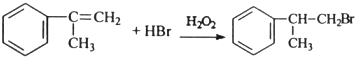 ;
; .
. ,最高价氧化物的化学式为:Cl2O7.
,最高价氧化物的化学式为:Cl2O7. .
. .
.


