题目内容
已知A为淡黄色固体,E、D为两种常见的用途很广的金属单质,H的溶液中含有两种金属阳离子,I不溶于水.

(1)写出下列物质的化学式:
A: ;
F: ;
G: ;
I: .
(2)证明H溶液中含有D2+离子,应选 ;
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
(3)按要求写方程式:
A与水反应的化学方程式: ;B与E反应的离子方程式: .

(1)写出下列物质的化学式:
A:
F:
G:
I:
(2)证明H溶液中含有D2+离子,应选
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
(3)按要求写方程式:
A与水反应的化学方程式:
考点:无机物的推断
专题:推断题
分析:A为淡黄色固体,能和水反应,则A是Na2O2,过氧化钠和水反应生成NaOH和氧气,E、D为两种常见的用途很广的金属单质,D能在C中燃烧,则C是O2,B是NaOH,能和NaOH溶液反应的金属单质是Al,二者反应生成偏铝酸钠和氢气,则E是Al,G能和二氧化碳反应,则G是NaAlO2,I不溶于水,则I是Al(OH)3,
F和盐酸反应生成H,H的溶液中含有两种金属阳离子,则D是Fe,F是Fe3O4,H是FeCl2、FeCl3,再结合题目分析解答.
F和盐酸反应生成H,H的溶液中含有两种金属阳离子,则D是Fe,F是Fe3O4,H是FeCl2、FeCl3,再结合题目分析解答.
解答:
解:A为淡黄色固体,能和水反应,则A是Na2O2,过氧化钠和水反应生成NaOH和氧气,E、D为两种常见的用途很广的金属单质,D能在C中燃烧,则C是O2,B是NaOH,能和NaOH溶液反应的金属单质是Al,二者反应生成偏铝酸钠和氢气,则E是Al,G能和二氧化碳反应,则G是NaAlO2,I不溶于水,则I是Al(OH)3,
F和盐酸反应生成H,H的溶液中含有两种金属阳离子,则D是Fe,F是Fe3O4,H是FeCl2、FeCl3,
(1)通过以上分析知,A、F、G、I分别是Na2O2、Fe3O4、NaAlO2、Al(OH)3,
故答案为:Na2O2;Fe3O4;NaAlO2;Al(OH)3;
(2)如果检验H中含有亚铁离子,亚铁离子具有还原性,能被酸性高锰酸钾氧化而使酸性高锰酸钾溶液褪色,故选d;
(3)A是过氧化钠,过氧化钠 和水反应生成氢氧化钠和氧气,反应方程式为2Na2O2+2H2O=4NaOH+O2↑,B是Al,E是NaOH,二者反应生成偏铝酸钠和氢气,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑;2Al+2OH-+2H2O=2AlO2-+3H2↑.
F和盐酸反应生成H,H的溶液中含有两种金属阳离子,则D是Fe,F是Fe3O4,H是FeCl2、FeCl3,
(1)通过以上分析知,A、F、G、I分别是Na2O2、Fe3O4、NaAlO2、Al(OH)3,
故答案为:Na2O2;Fe3O4;NaAlO2;Al(OH)3;
(2)如果检验H中含有亚铁离子,亚铁离子具有还原性,能被酸性高锰酸钾氧化而使酸性高锰酸钾溶液褪色,故选d;
(3)A是过氧化钠,过氧化钠 和水反应生成氢氧化钠和氧气,反应方程式为2Na2O2+2H2O=4NaOH+O2↑,B是Al,E是NaOH,二者反应生成偏铝酸钠和氢气,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑;2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评:本题以Al、Na、Fe及其化合物为载体考查了无机物推断,根据A的元素及性质确定A,再结合物质之间的反应、反应现象进行推断,题目难度不大.

练习册系列答案
相关题目
某元素的最高价含氧酸的阴离子符号是RO3-,则该元素的气态氢化物的化学式是( )
| A、HR |
| B、H2R |
| C、RH3 |
| D、不能确定 |
已知反应:2M(g)+N(g)+P(g)
2Q(g)+3R(g)△H>0,在恒容的密闭容器中,下列有关说法正确的是( )
| 180℃ |
| 催化剂 |
| A、平衡时,其他条件不变,增加M的浓度,N的转化率减小 |
| B、平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| C、单位时间内消耗N和Q的物质的量比为1:1时,反应达到平衡 |
| D、其他条件不变,使用高效催化剂,N和P的转化率增大 |

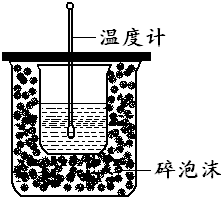 在如图所示的装置中进行中和反应的反应热测定,实验操作如下:
在如图所示的装置中进行中和反应的反应热测定,实验操作如下: