题目内容
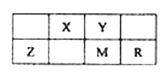
【题目】五种短周期元素在周期表中的位置如图所示,其中R元素原子的最外层电子数等于其电子层数的2倍,下列判断正确的是
A. 元素的非金属性次序为:Y>X>M
B. 气态氢化物稳定性:M>R
C. Z的氧化物可以做光导纤维
D. 最D高价氧化物对应水化物的酸性:Y>X
【答案】D
【解析】试题分析:由短周期元素在周期表的位置可知,X、Y处于第二周期,Z、M、R处于第三周期,R元素原子的最外层电子数等于电子层数的2倍,则R为S,可推知X为C元素,Y为N元素,Z为Al,M为P元素。A.磷酸的酸性碳酸的强,故非金属性P>C,故A错误;B.非金属性越强,气态氢化物越稳定,非金属性R>M,故氢化物稳定性:R>M,故B错误;C.Z的氧化物为三氧化二铝,可以用作耐火材料,用作光导纤维的是二氧化硅,故C错误;D.非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性Y>X,故最高价含氧酸酸性:Y>X,故D正确,故选D。

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案【题目】某工业流程中,进入反应塔的混合气体中NO和O2的物质的量分数分別为0.10和0.06,发生化学反应2NO(g)+O2(g) ![]() 2NO2(g),在其他条件相同时,测得实验数据如下表:
2NO2(g),在其他条件相同时,测得实验数据如下表:
压强/(×105Pa) | 温度/℃ | NO达到所列转化率需要时间/s | ||
50% | 90% | 98% | ||
1.0 | 30 | 12 | 250 | 2830 |
90 | 25 | 510 | 5760 | |
8.0 | 30 | 0.2 | 3.9 | 36 |
90 | 0.6 | 7.9 | 74 | |
根据表中数据,下列说法正确的是
A.升高温度,反应速率加快
B.增大压强,反应速率变慢
C.在1.0×105 Pa、90℃条件下,当转化率为98%时反应已达平衡
D.若进入反应塔的混合气体为a mol,反应速率以![]() 表示,则在8.0×105Pa、30℃条件下,转化率从50%增至90%时段NO的反应速率为
表示,则在8.0×105Pa、30℃条件下,转化率从50%增至90%时段NO的反应速率为![]() mols-1
mols-1
【题目】二氧化氯(ClO2)是世界卫生组织(WHO)推荐的A1级广谱、安全、高效消毒剂。以下是ClO2的两种制备方法:
方法一:2NaClO3 + 4HCl → 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O
方法二:H2C2O4 + 2NaClO3 + H2SO4 → Na2SO4 + 2CO2↑ + 2ClO2↑ + 2H2O
完成下列填空:
(1)在方法一中,当有0.2 mol电子发生转移时,参与反应的还原剂为_________ mol。
(2)在方法二中,反应物H2C2O4_________(填序号)。
a.仅做氧化剂 b.既被氧化又被还原
c.发生氧化反应 d.既未被氧化也未被还原
(3)两种方法相比,___________(填写“方法一”或“方法二”)制备的ClO2更适合用于饮用水的消毒,其主要原因是______________________________________________。
(4)实验室也可用氯酸钠(NaClO3)和亚硫酸钠(Na2SO3)用硫酸酸化,加热制备二氧化氯,其化学反应方程式为 ________________________________________________。
(5)氯原子核外共有______种不同运动状态的电子,氯离子的最外层电子排布式是________。
(6)CCl4分子的空间构型为__________________,CO2的电子式是___________________。
(7)相同压强下,部分元素氯化物的熔点见表:
氯化物 | NaCl | KCl | CCl4 |
熔点/℃ | 804 | 773 | -22.92 |
试解释表中氯化物熔点差异的原因:_______________________________________________________。