题目内容
3.为了测定某有机物A的结构,做如下实验:①将2.3g该有机物完全燃烧,生成0.1molCO2和2.7g水;
②用核磁共振仪处理该化合物,得到谱图只有一个峰.
试回答下列问题:
(1)有机物A的实验式是C2H6O.
(2)能否根据A的实验室确定A的分子式?能(填“能”或“不能”),若能,则A的分子式是C2H6O(若不能,则此空不填).
(3)写出有机物A可能的结构简式:CH3OCH3.
分析 (1)根据n=$\frac{m}{M}$计算生成的水的物质的量,计算碳元素、氢元素的质量,根据质量守恒判断有机物A是否含有氧元素,若含有氧元素,计算氧元素质量、氧原子物质的量,根据有机物A中C、H、O原子个数比值确定最简式;
(2)若最简式中H原子已经饱和碳的四价结构,则最简式即为分子式;
(3)A的核磁共振氢谱只有一个吸收峰,则有机物A含有1种H原子,结合分子式书写可能的结构简式.
解答 解:(1)2.3 g该有机物中,n(C)=n(CO2)=0.1 mol,含有的碳原子的质量为m(C)=0.1 mol×12 g•mol-1=1.2 g,氢原子的物质的量为:n(H)=$\frac{2.7g}{18g/mol}$×2=0.3 mol,氢原子的质量为m(H)=0.3 mol×1 g•mol-1=0.3 g,该有机物中m(O)=2.3 g-1.2 g-0.3 g=0.8 g,氧元素的物质的量为n(O)=$\frac{0.8g}{16g/mol}$=0.05 mol,则n(C):n(H):n(O)=0.1 mol:0.3 mol:0.05 mol=2:6:1,所以A的实验式是C2H6O,
故答案为:C2H6O;
(2)该有机物的最简式为C2H6O,H原子已经饱和C原子的四价结构,最简式即为分子式,
故答案为:能;C2H6O;
(3)A的核磁共振氢谱只有一个吸收峰,则有机物A含有1种H原子,其结构简式为:CH3OCH3,
故答案为:CH3OCH3.
点评 本题考查有机物分子式与结构确定等,难度中等,侧重对基础知识与学生综合能力考查,注意“最简式中H原子已经饱和碳的四价结构,则最简式即为分子式”.

练习册系列答案
相关题目
18.要制取相同质量的Cu(NO3)2,下列反应中消耗HNO3最少的反应是( )
| A. | Cu和浓HNO3 | B. | Cu和稀HNO3 | C. | CuO和HNO3 | D. | Cu2O和HNO3 |
 NH3•H2O+H+(用离子方程式表示);室温时,向(NH4)2SO4,溶液中滴人NaOH 溶液至溶液呈中性,则所得溶液中微粒浓度大小关系c(Na+)=c(NH3•H2O).(填“>”、“<”或“=”)
NH3•H2O+H+(用离子方程式表示);室温时,向(NH4)2SO4,溶液中滴人NaOH 溶液至溶液呈中性,则所得溶液中微粒浓度大小关系c(Na+)=c(NH3•H2O).(填“>”、“<”或“=”) ,C元素最高价氧化物对应的水化物的电子式
,C元素最高价氧化物对应的水化物的电子式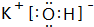 .
. .
.
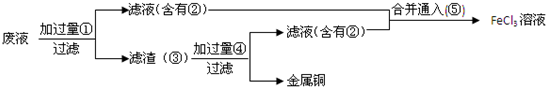
 和足量氢氧化钠溶液反应:
和足量氢氧化钠溶液反应: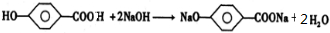
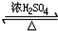 CH3OOCCOOCH3+2H2O
CH3OOCCOOCH3+2H2O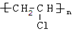 .
.