题目内容
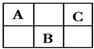 A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子的原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子的原子核内质子数和中子数相等.(1)写出A、B、C三种元素的元素符号:
(2)下列叙述正确的是
A.最高价氧化物对应水化物的酸性:C>B
B.C单质是氧化性最强的非金属单质
C.A的氢化物中具有一定的还原性
D.B在第三周期ⅦA族
(3)B原子的质量数是
(4)写出A的气态氢化物与A的最高价氧化物对应水化物反应的化学方程式
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A、B、C为短周期元素,由它们在周期表中的位置,可知A、C处于第二周期,B处于第三周期,令A原子核外电子为x,则B质子数为x+9,C核外电子数为x+2,则:x+x+2=x+9,解得x=7,故A为N元素、B为S元素、C为F元素,据此解答.
解答:
解:A、B、C为短周期元素,由它们在周期表中的位置,可知A、C处于第二周期,B处于第三周期,令A原子核外电子为x,则B质子数为x+9,C核外电子数为x+2,则:x+x+2=x+9,解得x=7,故A为N元素、B为S元素、C为F元素,
(1)由上述分析可知,A为N元素、B为S元素、C为F元素,故答案为:N;S;F;
(2)A.C为氟元素,没有正化合价,故A错误;
B.C为F元素,非金属性最强,单质是氧化性最强的非金属单质,故B正确;
C.A的氢化物为氨气,N元素处于最低价,氨气具有一定的还原性,故C正确;
D.B为S元素,处于第三周期ⅥA族,故D错误,
故答案为:BC;
(3)B为S元素,原子核内质子数和中子数相等,故其质量数为16+16=32;C为F元素,原子核外有9个电子,各层电子数为2、7,原子的原子结构示意图为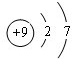 ,
,
故答案为:32;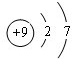 ;
;
(4)氨气与硝酸反应生成硝酸铵,反应的化学方程式为:NH3+HNO3=NH4NO3,
故答案为:NH3+HNO3=NH4NO3.
(1)由上述分析可知,A为N元素、B为S元素、C为F元素,故答案为:N;S;F;
(2)A.C为氟元素,没有正化合价,故A错误;
B.C为F元素,非金属性最强,单质是氧化性最强的非金属单质,故B正确;
C.A的氢化物为氨气,N元素处于最低价,氨气具有一定的还原性,故C正确;
D.B为S元素,处于第三周期ⅥA族,故D错误,
故答案为:BC;
(3)B为S元素,原子核内质子数和中子数相等,故其质量数为16+16=32;C为F元素,原子核外有9个电子,各层电子数为2、7,原子的原子结构示意图为
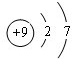 ,
,故答案为:32;
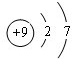 ;
;(4)氨气与硝酸反应生成硝酸铵,反应的化学方程式为:NH3+HNO3=NH4NO3,
故答案为:NH3+HNO3=NH4NO3.
点评:本题考查原子结构与元素周期表,难度不大,推断元素是解题关键,注意理解同主族元素原子序数关系.

练习册系列答案
相关题目
下列有关物质性质和应用的说法均正确的是( )
| A、常温下二氧化硅不与任何酸反应,可用石英容器盛放氢氟酸 |
| B、常温下浓硝酸与铁不反应,可在常温下用铁罐贮运浓硝酸 |
| C、锌的金属活泼性比铁的强,可在铁船闸上装锌块减缓腐蚀 |
| D、氧化铝熔点很高,可用氧化铝制造坩埚融化氢氧化钠 |
下列各组离子在指定溶液中能大量共存的是( )
| A、加入稀硝酸的溶液:K+、Cl-、HS-、SO32- |
| B、加入FeCl3溶液:I-、NH4+、Cl、Ba2+ |
| C、加入NaOH的溶液:Na+、AlO2-、CO32-、K+ |
| D、无色pH=12的溶液:Fe3+、Mg2+、Al3+、NO3- |
 常温下,向20mL x mol?L-1 CH3COOH溶液中逐滴加入等物质的量浓度的
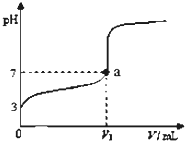
常温下,向20mL x mol?L-1 CH3COOH溶液中逐滴加入等物质的量浓度的NaOH溶液,混合液的pH随NaOH溶液的体积(V)变化关系如图所示(忽略温度变化).下列说法中不正确的是( )
| A、上述 CH3COOH溶液中:c(H+)=1×10-3mol?L-1 |
| B、图中V1>20mL |
| C、a点对应的溶液中:c(CH3COO-)=c(Na+) |
| D、加入NaOH溶液体积为20 mL时,溶液中:c(CH3COOH)+c(H+)=c(OH-)+c(CH3COO-) |
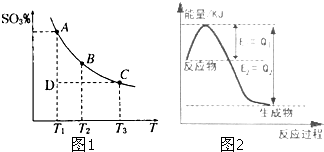 运用化学反应原理研究元素及其化合物的反应有重要意义.
运用化学反应原理研究元素及其化合物的反应有重要意义.